北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
「WB急救室」杂带多、非特异条带泛滥?6个"背锅侠"竟是实验老手!
52 人阅读发布时间:2026-03-24 17:15
WB,Western Blot
一个科研界的「神级」实验,科研人的「老朋友」
却总是不经意的给你带来「致命痛苦」
从特异性结合到胡乱贴标的惊心演变
总是让人猝不及防
WB结果如同开“盲盒”,杂带多、非特异性条带出现的概率也很大,让我们一起看看有哪6个“背锅侠”吧!
1,蛋白样品的“锅”有点大
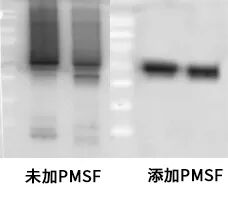
1)需要通过BCA或Bradford法精确测定蛋白浓度,然后根据蛋白浓度选择等质量或等体积上样。WB每条泳道总蛋白的上样量通常为20-50μg,磷酸化蛋白可能需要50μg。保证蛋白质量的同时,上样体积不宜过多,一般为5-10μL。
2)细胞裂解前加入蛋白酶抑制剂,如PMSF、AEBSF、抑肽酶等。裂解过程要低温、快速,如采用冰浴超声多次短暂循环方法,打1-3秒停2-5秒,重复5-10次。
3)查阅文献和数据库,进行生物信息学分析,确定蛋白质的修饰位点信息,比如磷酸化、乙酰化、甲基化、糖基化等。可以对样品进行去修饰化处理验证,加入磷酸酶、糖苷酶等酶。或使用未修改的纯化蛋白、敲除目的蛋白的细胞样本作为阴性对照。用5% BSA替代脱脂奶粉封闭,可减少磷酸化或糖基化的非特异性结合。
4)针对目的蛋白存在多个亚型,可选择靶向亚型独特区域的抗体,如N端或C端可变区。使用高浓度分离胶(如15%)提高分辨率。使用Image Lab软件对多条带分别定量,结合总蛋白归一化法(如Stain-Free技术)校正表达量。
5)如果细胞传代次数过多,会造成蛋白表达模式发生分化,出现非特异性结合,建议用原代细胞和待测样品细胞一起做对照实验。
2,一抗的“锅”也要查一下
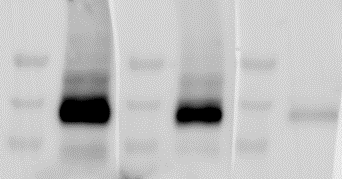
解决方案
1)根据抗体说明书或官网信息,确认此抗体是否适合用于WB实验及其特异性。
2)按照抗体说明书,选择合适的稀释液和保存温度。常用的稀释液包括PBS、TBST或市售抗体专用稀释液。一般建议抗体保存在-20℃。分装是避免抗体降解和污染的有效方法,分装量不应少于10μL。具体需以抗体说明书为准,建议在使用前咨询厂商技术支持进行确认。
3)根据抗体说明书推荐浓度范围,进行浓度梯度优化实验。稀释液使用含有5%脱脂奶粉或BSA的TBST缓冲液,可减少非特异性结合。
4)建议首次使用新抗体时,平行设置4℃与37℃孵育组,对比选择最佳条件。一般建议一抗4℃过夜孵育,如果赶时间,可以室温孵育2h。高温(如37℃)会加速抗体与蛋白的分子碰撞,增加抗体与非目的蛋白结合的概率,或者造成蛋白样品、抗体发生构象变化,暴露非特异性结合位点。可根据抗体类型和目标蛋白丰度,进行不同温度不同时间段的优化实验。仅加二抗孵育可排除二抗非特异性结合。使用同种属同亚型的非靶点抗体做同型对照,验证目的蛋白的特异性。
3,封闭的“锅”也常见
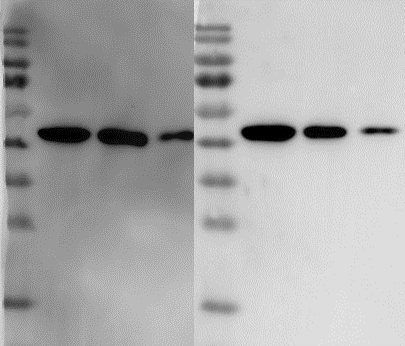
在Western blot(WB)实验中,封闭是阻断膜上非特异性结合的关键环节。封闭液中含有一些非特异性蛋白质或其他分子,可与膜表面的非特异性结合位点结合,从而减少抗体与膜的非特异性结合,降低背景信号。常用5% 脱脂奶粉或3% BSA室温封闭1小时或4℃过夜。添加0.1% Tween-20能减少非特异性结合。对于高丰度蛋白样品可先5%脱脂奶粉封闭30分钟,再切换至3% BSA封闭1小时。当然低丰度蛋白样品需要缩短封闭时间,如室温30分钟。
4,洗膜有时也背锅
在WB实验中,洗膜不充分(时间过短或次数不足)会导致膜上残留抗体,增加非特异性结合和背景信号。建议使用pH值稳定的TBST缓冲液,将Tween-20的浓度从0.1%提升至0.2%-0.5%,减少非特异性结合。延长单次洗膜时间,比如从5分钟到10分钟,减少疏水结合。
5,电泳缓冲液偶尔也“背锅”
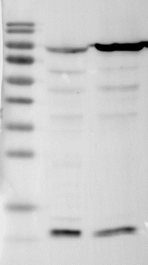
电泳液一般新鲜配制,用上2-3次就换了吧。配制之前需要查看试剂是否过期、浓缩液是否长菌、固体颗粒是否完全溶解,可用0.22μm滤膜除菌过滤。
6,显影的锅“偶现”

曝光强度过高或者曝光时间太久,会增加背景信号。显影液需现用现配,在30分钟内使用。根据显影液推荐范围设定曝光时间,比如从5秒开始,逐步延长至30秒、1分钟、5分钟等。






