北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
「WB急救室」开诊,条带开口笑、拖尾、重影、弯曲、哑铃状、波浪线,可能是电泳过程出问题了
326 人阅读发布时间:2026-03-24 17:09
电泳在Western Blot中具有核心作用,是实验成功的基础,是优秀蛋白质选手脱颖而出的“大舞台”。电泳液、电压电流、凝胶3大元素贯穿整个电泳过程。某个细节的失误,可能就会让条带直接翻车成表情包:微笑条带让你怀疑“蛋白成精了”、哑铃状的怕是刚跑完马拉松、拖尾的如同被老板骂哭的打工人,更刺激的是,电泳液漏了……
电泳就像爱情,电压过猛容易“擦枪走火”,条件太弱只能“暗送秋波”,只有精准把控,才能收获完美“蛋白CP”。来,测一测你的电泳段位:
✦ 一级:电泳液配置靠蒙
✦ 二级:条带拖尾能解释
✦ 三级:根据条带形状写段Rap
言归正传,我们来说一说怎么解决电泳条带“表情包”的问题吧。
问题一:不合时宜的微笑或皱眉

1)电泳液一般新鲜配制,用上2-3次就换了吧。配制之前需要查看试剂是否过期、浓缩液是否长菌、固体颗粒是否完全溶解,可用0.22μm滤膜除菌过滤。
2)凝胶最好现用现配,凝固时间受凝胶类型、浓度、环境温度及促凝剂状态等多因素影响。分离胶凝固后,凝胶与玻璃板接触面可见清晰折射线,无液体流动。为了防止分离胶氧化加快凝固,一般用无离子水、异丙醇、无水乙醇来封闭。建议用无水乙醇,残留少无异味。凝固后立即倒掉封闭液,并用滤纸吸干残留液体,避免长时间接触导致胶面变形。吸干残留液体后灌注浓缩胶。加入较高浓度TEMED(如0.1%),可加速凝固。胶液倒入后立即插入梳子,避免胶面凝固导致孔道不平。
|
凝胶类型 |
凝固时间 |
|
|
分离胶 |
低浓度(<8%) |
20-25分钟 |
|
浓度8%-12% |
约30分钟 |
|
|
高浓度(>12%) |
40-50分钟 |
|
|
浓缩胶 |
15-20分钟 |
|
温度会影响凝胶凝固。比如将配好的聚丙烯酰胺凝胶置于37℃温箱中20-30分钟,可加速凝固。低于20℃,可适当延长20-30分钟。凝胶长时间不用可以加点水密封后放到4℃保存。
3)电压设置参考每厘米2-5V的原则,比如20cm电泳槽可设为60-100V。建议采用两段式电泳:
浓缩胶阶段:80V恒定电压,以溴酚蓝指示剂迁移为参考,约20-30分钟,使样品压缩成平直条带。
分离胶阶段:120-150V。溴酚蓝迁移至凝胶底部,约60-90分钟,提升蛋白分辨率。
若凝胶浓度>12%,需适当降低电压(如100V)。大分子量蛋白(>100 kDa)可延长分离胶时间,120V下运行90-120分钟。高电压运行时,若电流>70mA,建议暂停电泳散热或降低电压。4°C环境电泳或使用循环冷却装置以防电泳过热。
4)除了电泳过程中的问题,蛋白样品间浓度差异大或盐离子浓度差异大也可能出现“微笑”条带。建议在上样前,通过BCA或Bradford法精确测定蛋白浓度,然后根据蛋白浓度选择等质量或等体积上样。
问题二:笑到腮帮子裂开

问题三:感觉被压榨了,条带呈哑铃状
如上,凝胶现用现配,溶液充分溶解、混匀。
如果排除凝胶问题,可以考虑对蛋白样品进行处理。比如使用0.45μm或0.22μm孔径的滤膜过滤,去除微小颗粒。将样品于4°C、12,000-16,000g离心15-20分钟,去除细胞碎片、未溶解组织块等大颗粒杂质。如果样品黏度过高,可能是含有大量核酸,可以在裂解液中加入全能核酸酶,37°C孵育15分钟,减少核酸与蛋白结合形成的复合物。
问题四:条带飘忽不定,起起伏伏
1)电压设置参考上文。将电泳槽置于冰水混合物中或连接循环冷却泵,持续降低电泳槽温度,维持缓冲液温度≤15°C。
2)凝胶凝固不均一也可能会出现波浪形条带,可以按照上文提到的方法进行优化。
3)如果样品中含有细胞碎片或DNA也可能会出现这种情况,可以如上文提到的进行离心、加核酸酶等处理蛋白样品。
4)还有一种情况是转膜过程中,夹得过紧或产热过多,导致凝胶变形,造成条带扭曲。夹紧时需施加均匀压力,以玻璃棒能滚动通过且无明显阻力为宜。反复使用的海绵垫易变形,建议每5次更换新垫。常规转膜设置为恒流模式200-300mA(膜面积10×10cm),时间1-2小时。若目标蛋白>100kDa,需降低电流至150-200mA并延长转膜时间。转膜前将缓冲液置于4°C预冷,转膜槽置于冰水混合物,可降低转膜过热风险。
还有一个小技巧,在转膜液中加20%甲醇,不仅可以活化PVDF膜。还能减少凝胶溶胀导致的夹紧压力。
问题五:条带如同哈雷彗星,拖着长长的尾巴
1)凝胶现用现配,溶液充分溶解、混匀。
2)配制新鲜的电泳缓冲液,尤其是检查各种试剂是否过期(长毛的Tris-HCl真的就别用了呀!)。电泳缓冲液pH不对会影响蛋白迁移速率,常用Tris-甘氨酸缓冲液pH为8.3-8.5。
3)电泳设置合适的电压,防止产热严重造成拖尾,建议采用如上提到的两段式电泳。
4)其他如上样量大、浓度高、含有聚集体、降解、糖基化修饰等样品原因造成的条带拖尾,可以查看「WB急救室」的相关文章,这里不再赘述。
问题六:个别条带扭曲变形
1)如上文,根据凝胶类型、浓度、环境温度,选择充足的时间让凝胶完全凝固。
2)制胶时,充分混匀凝胶液后从胶板一侧缓慢加入凝胶液,每次加入移液枪中90%液体即可,避免产生气泡。
3)配制分离胶时,使用无水乙醇进行液面压平,也可除去气泡。
4)浓缩胶尽量加满胶板,梳子从两侧同时按下,避免产生气泡。
5)制胶前,充分刷洗玻璃板和梳子。用中性洗洁精可去除干涸胶体或颗粒杂质。然后用自来水冲洗至无泡沫,再用去离子水冲洗2-3次。可垂直晾干或用吹风机吹干,避免毛巾擦拭引入纤维。用无水乙醇去除有机残留物,如油渍、指纹等。
问题七:条带上坡或下坡
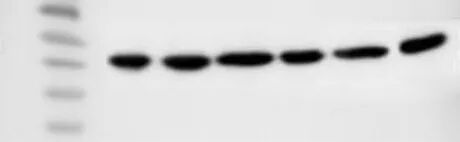
电泳槽漏液的几率较大。电泳槽漏液会导致电流异常、条带扭曲。灌胶前在电泳槽中加入清水,观察30分钟是否有渗漏。溴酚蓝指示带出现“笑脸”或“皱眉”状变形,可能是漏液导致。玻璃板要彻底干燥后再组装,塑料夹子需均匀施力,避免过松或过紧导致变形。密封条一般使用50次或弹性下降后进行更换。电极丝可以每月用无水乙醇擦拭,防止氧化。
|
漏液位置 |
常见原因 |
解决方案 |
|
玻璃板边缘 |
玻璃板磕碰破损、夹子未拧紧或密闭不良 |
更换新的玻璃板或压片,清洗接触面并重新夹紧 |
|
密封条处 |
老化、安装错位或表面凹凸不平 |
更换密封条,安装时自然嵌入槽内,避免拉扯 |
|
电极孔处 |
密封圈磨损或螺丝未拧紧 |
更换密封圈,粘接开胶处 |
|
底部胶体连接处 |
玻璃板未对齐或胶未完全凝固 |
重新制胶,确保凝固时间充足 |
问题八:条带有重影或呈梳子状
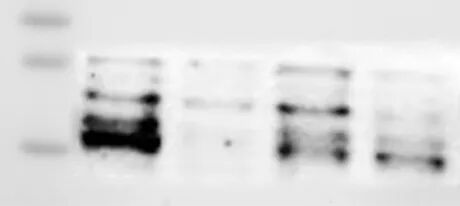
1)如上文,根据凝胶类型、浓度、环境温度,选择充足的时间让凝胶完全凝固。
2)凝胶长时间不用可以加点水密封后放到4℃保存。当然现用现配会更好。
3)更换新的PVDF膜。
问题九:出现多条非特异性条带
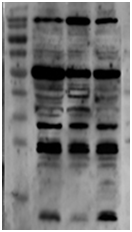
电泳缓冲液长菌造成非特异条带的情况比较少见,以下情况可能更常见:
1)蛋白样品降解成多个蛋白,而这些蛋白同样可能被一抗识别。
2)目的蛋白存在多种修饰方式,如乙酰化、甲基化、糖基化、磷酸化、烷基化等。
3)目的蛋白有多个亚型,分子量存在差异。
4)一抗特异性差、降解、使用次数过多。
5)PVDF膜封闭时间不足,或者封闭液失效
6)洗膜时间过短或者次数不足,PVDF膜上残留一抗
其他原因造成的条带异常,如蛋白样品降解、浓度高、抗体不合适等,将会在「WB急救室」专题其他文章中进行详细讲述,欢迎大家订阅专题,查看相关改进方案。






