北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
「WB急救室」翻车图鉴:毛玻璃状、有脏东西、小黑点、反白、泡泡……该反思一下转膜过程了!
304 人阅读发布时间:2026-03-24 16:38
Human, Mouse, Rat, Rabbit
如何实现从SDS-PAGE凝胶到PVDF膜的完美迁移?
毛玻璃条带、斑斑点点的小黑点、冒泡、有点脏……
膜上时不时的来个“意外之客”,
让科研人在深夜崩溃。
「WB急救室」第6期:直击转膜十大翻车现场,只需五招轻松避坑:选好膜、做好“三明治”、设好电流、降温到位、溶液新无污染。
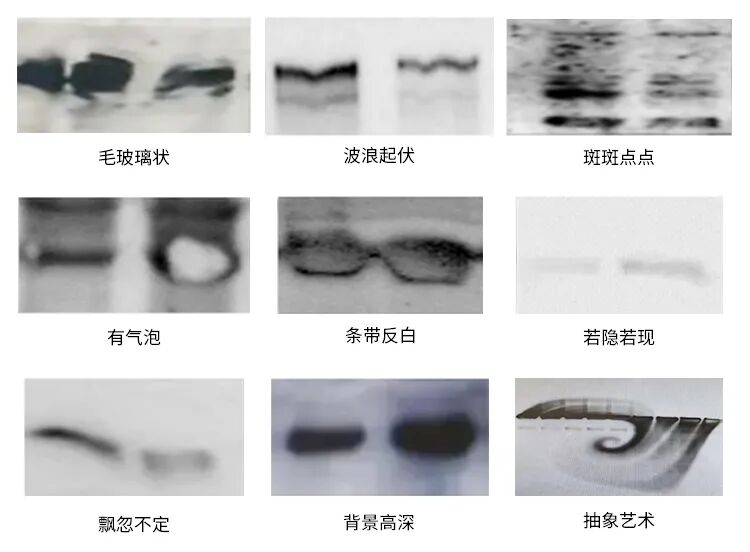
问题一:条带呈毛玻璃状
1)转膜时夹得太紧或太松会导致凝胶接触不良或者变形。确保“三明治”结构平整,如湿转法依次放置海绵(2层)-滤纸(3层)-胶-膜-滤纸(3层)-海绵(2层),半干转法的滤纸总厚度不超过夹板高度的2/3。排除气泡后用力压紧夹板,定期更换海绵或添加滤纸衬垫。过度夹紧会压碎凝胶,尤其是低浓度胶(<8%),导致蛋白条带扭曲或断裂。
判断转膜松紧度的标准:
|
查看指标 |
松紧适宜表现 |
异常表现(过松或过紧) |
|
夹板闭合状态 |
能自然闭合且无缝隙 |
需外力强压闭合或易晃动 |
|
滤纸边缘状态 |
整齐无褶皱 |
过松:翘起,过紧:压痕深 |
|
转膜后胶体状态 |
完整无碎裂 |
过紧:胶压缩变形或断裂 |
2)转膜过程防止放热过多导致凝胶变形。常规转膜设置为恒流模式200-300mA(膜面积10×10cm),时间1-2小时。高分子量蛋白(>150kDa)可采用梯度转膜方法,先以200mA恒流转膜30分钟转移小分子量蛋白,再切换至350mA恒流1小时转移大分子量蛋白。低分子量蛋白(<50kDa)需缩短转膜时间至45-60分钟。湿转法推荐100V恒压,配合冰浴维持温度≤15℃,半干转法设置25V恒压,总时间≤60分钟。海绵层数控制在4-6层,使用高密度3mm厚滤纸,提高散热效果。配备冷却装置,如湿转槽外包裹循环冰袋,内置冷却棒。
3)凝胶预处理防止其破碎。电泳后可以将凝胶浸泡于含有20%甘油的转移缓冲液15分钟,增强胶的韧性。在转移缓冲液中添加20%甲醇,可减少凝胶膨胀并增强蛋白与膜的结合。低浓度胶(如8%)可用0.5%琼脂糖封边,防止边缘变形。建议使用预冷刀片切割凝胶,减少热应力导致的裂纹。
4)PVDF膜存在问题,如湿润不均匀、过期、存在污染物、损坏等。未充分湿润的PVDF膜表面有疏水区域残留,蛋白结合不均,导致条带呈现波浪状或局部缺失。如果膜上有黑点,可能是封闭液有颗粒或膜上有颗粒污染物。如果条带间出现垂直黑线,可能是镊子夹取时造成的机械损伤或膜表面撕裂。过期膜的孔结构塌陷,封闭液无法有效填充孔隙,导致抗体非特异性结合。
|
问题描述 |
检测方法 |
优化措施 |
|
湿润不均 |
丽春红预染色观察结合均匀性 |
甲醇激活延长至1分钟 |
|
膜过期 |
与新的膜比较封闭效果 |
储存时密封避光,6个月内使用 |
|
污染物 |
白炽灯侧光检查膜表面 |
封闭液用0.22μm滤膜过滤 |
|
物理损伤 |
显微镜观察膜完整性 |
使用钝头镊子,转膜前检查海绵垫 |
问题二:条带波浪起伏
问题三:膜上有小黑点
问题四:条带上有泡泡
问题五:条带正常,但膜上有脏东西
试剂污染主要是封闭液和缓冲液问题。封闭液中有未溶颗粒会在膜上形成黑点,缓冲液长菌会造成如图所示结果,建议用0.45μm滤膜过滤封闭液以除去颗粒,配制新鲜的缓冲液并用0.22μm滤膜过滤除菌。
抗体污染会出现非特异性条带或斑点。建议降低一抗或二抗浓度,缩短孵育时间。
操作不当会造成膜未充分浸泡(干燥导致局部污染)或转膜气泡残留。孵育和洗膜时确保膜完全浸没,避免局部干燥。转膜时用玻棒赶走滤纸与膜之间的气泡。戴手套操作膜,避免直接接触。
问题六:条带反白
1)做到全程浸润。从转膜到显影的所有步骤,确保膜始终浸在液体中,比如缓冲液至少5 mL/cm²,孵育盒加盖,孵育盒底部垫湿滤纸。
2)优化操作时长。提前准备好封闭液和抗体稀释液,缩短转移间隔时间。提前将TBST、封闭液等置于冰上备用。将实验分为“转膜-封闭”和“抗体孵育-显影”两个阶段,减少中间停顿。使用计时器严格控制每步操作时间,如洗涤过程,5分钟x5次。
3)控温控光。在4℃环境下进行孵育步骤,孵育时低速振荡(如30 rpm)可避免局部干燥。关闭实验台强光源,避免膜局部受热。
如果发现膜已干燥,可以按以下步骤进行抢救:
首先,用含0.1% Tween-20的TBST轻柔冲洗膜表面。
接着,用100%甲醇浸泡PVDF膜10秒后转至TBST。
最后,更换新鲜封闭液重新“封印”,推荐用5% BSA,时间延长至2小时。
问题七:条带弱
WB实验中,膜的种类、孔径会影响转移到膜上的蛋白量。
NC(硝酸纤维素)膜物理吸附能力比PVDF膜弱,尤其对疏水性蛋白或小分子量蛋白吸附效果差,适合大分子量蛋白(>20 kDa)的转移。小分子量蛋白(<20 kDa)和疏水性蛋白建议用PVDF膜。当然,PVDF膜需要用甲醇或乙醇充分活化,以提高蛋白结合能力。
膜的孔径会影响蛋白捕获效率,比如使用0.45 μm孔径的NC膜转移小于20 kDa的蛋白,孔径过大而使蛋白穿孔而过,不留痕迹。因此,大于20 kDa的蛋白选择0.45 μm孔径的NC膜更经济实惠,小于20 kDa的蛋白优先选择0.22 μm孔径的PVDF膜,极小蛋白(<10 kDa)可叠加两张0.22 μm膜,以提高捕获率。
转膜后用考马斯亮蓝染色凝胶,以确认蛋白残留量。用丽春红短暂染色膜表面,观察蛋白分布是否均匀。
问题八:背景高
建议使用新鲜配制的转膜液,并在使用前通过0.2微米滤器过滤。不用时置于-20℃保存,有絮状物沉淀就别用了。
问题九:条带飘逸不定
电压或电流不稳定,建议从电源、转膜液和设备三方面系统排查。
定期清洁电极、检查电源线连接。长期使用的电极可能因腐蚀或表面附着杂质(如盐结晶)导致接触不良,可以用乙醇擦拭电极表面,严重腐蚀时更换新电极。转膜过程优先选择恒流模式,避免因电阻变化导致电压波动。
转膜液重复使用会导致离子强度下降、pH异常、甲醇挥发,造成恒流模式下电压“狂飙”或恒压模式下电流逐渐下降,影响蛋白迁移效率。建议转膜液使用次数不超过3次,每次补充10-20%甲醇。
“三明治”要规范整齐,滤纸尺寸与凝胶一致,过大会导致电流“短路”。冰浴转膜或使用循环冷却系统降低转膜系统温度,避免缓冲液发热和减少甲醇挥发。
问题十:条带亮度不均一,忽明忽暗






