北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
「新品速递」通用型Whitlow218 Linker兔单抗,高效助力CAR流式细胞检测
552 人阅读发布时间:2025-08-21 15:15
引言
CAR-T细胞疗法在血液肿瘤治疗中屡创奇迹,目前正在实体瘤领域“开疆拓土”。2025年6月1日,The Lancet(柳叶刀)发表北京大学沈琳教授团队主导的全球CLDN18.2 CAR-T 胃癌随机对照研究的阳性结果:无进展生存期显著延长,总生存期延长44%。近年来CAR-T在系统性红斑狼疮、多发性硬化症等自身免疫性疾病领域展现出巨大的潜力。
但是,在CAR-T研发进程中,长期面临一个棘手的难题。每一种新CAR靶向肿瘤新抗原设计,需要每一次迭代开发相应的经独特验证的检测试剂,以确定CAR表面表达。这一过程不仅成本高昂、费时费力,还可能因抗体特异性不足导致数据偏差,严重拖慢项目进度。
如今,这一难题迎来了“通用型”的解决方案。义翘神州推出全新的Whitlow218 Linker兔单抗,特异性结合scFv片段重链和轻链间的Whitlow218 Linker序列。Whitlow218 Linker兔单抗不区分CAR-T靶点,具有多靶点多CAR结果通用的特点。兔单抗还具有高亲和力、高特异性的优势。义翘神州已成功开发FITC、PE标记的适用于流式细胞术的单克隆抗体,APC、AF488、AF647、Biotin等标记的抗体也在开发中,将会陆续上线。
CAR表达检测:CAR-T疗效评估与质量控制的核心
在详细了解抗CAR Linker单抗这一新颖的检测技术之前,我们先简单复习一下CAR-T细胞的结构和功能。
CAR(嵌合抗原受体)是一种经过基因工程改造的受体,结合了抗体的抗原识别能力与T细胞激活功能。CAR主要由四部分组成:
1)胞外抗原结合结构域:CAR的核心区域,负责识别肿瘤细胞表面的特定抗原。通常为单链可变片段(scFv)或抗原结合区,具有高度特异性。
2)铰链结构域:连接抗原结合结构域及跨膜结构域,有助于维持抗原结合域的空间构象,促进抗原结合效率。
3)跨膜结构域:确保受体嵌入T细胞膜,保持其稳定性和功能性。
4)胞内信号传导结构域:CAR激活T细胞的关键,一般为CD3ζ或CD3ε等T细胞受体的胞内结构域,以及共刺激分子CD28、4-1BB等,可以增强T细胞的持久性和抗肿瘤活性。
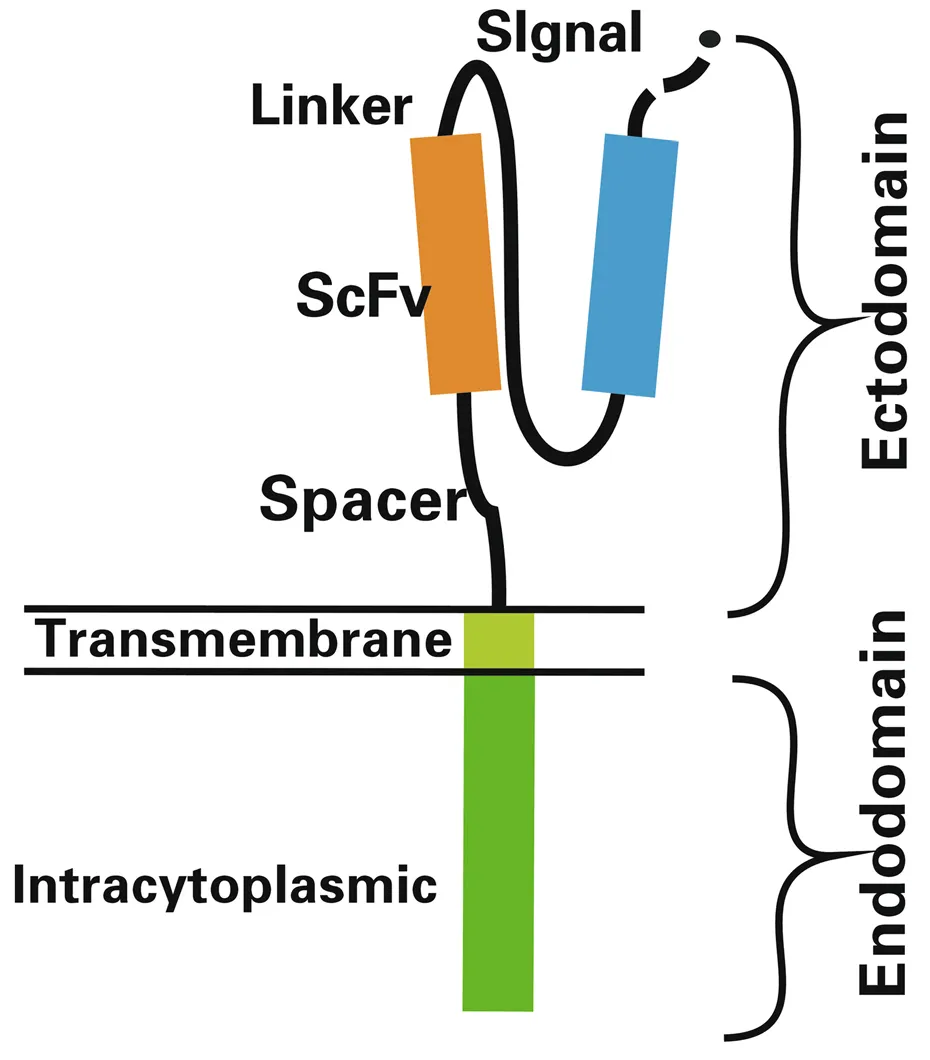
CAR结构示意图(源自文献:doi: 10.1186/s40364-017-0102-y)
CAR细胞阳性率是评估CAR-T细胞产品活性的重要指标,直接影响对肿瘤靶点的识别能力和杀死效应。CAR-T细胞回输到患者体内,检测其在外周血或组织中的CAR表达情况,有助于评估细胞的扩增能力和体内持久性,对判断治疗反应、疗效持续性乃至复发风险具有重要参考价值。同时,动态检测CAR-T细胞表达变化,可评估其潜在免疫原性及安全风险。因此,建立一套灵敏、可靠、通用的CAR表达检测系统,对CAR-T细胞疗法的开发和评价至关重要。
目前,获批上市的CAR-T细胞靶向CD19或BCMA,所以在CAR-T患者诊断中,以重组人BCMA或CD19蛋白检测CAR的流式细胞术占据主导地位。这种方法精确性和特异性很高,但仅限于检测单一特定靶点,不适合CAR-T筛选发现及临床前研究。
科研人员已开发多种CAR检测方法,比如结合到免疫球蛋白的Protein L,或结合到抗体Fc段的多克隆抗体。Protein L与免疫球蛋白κ轻链结合,不能检测包含λ链的CAR。多克隆抗体可能与患者自身IgG发生交叉反应,导致假阳性。还有抗独特型抗体,与CAR抗原结合区独特位结合,具有高度的特异性和敏感型,背景染色较低,但是抗独特型抗体难获得。
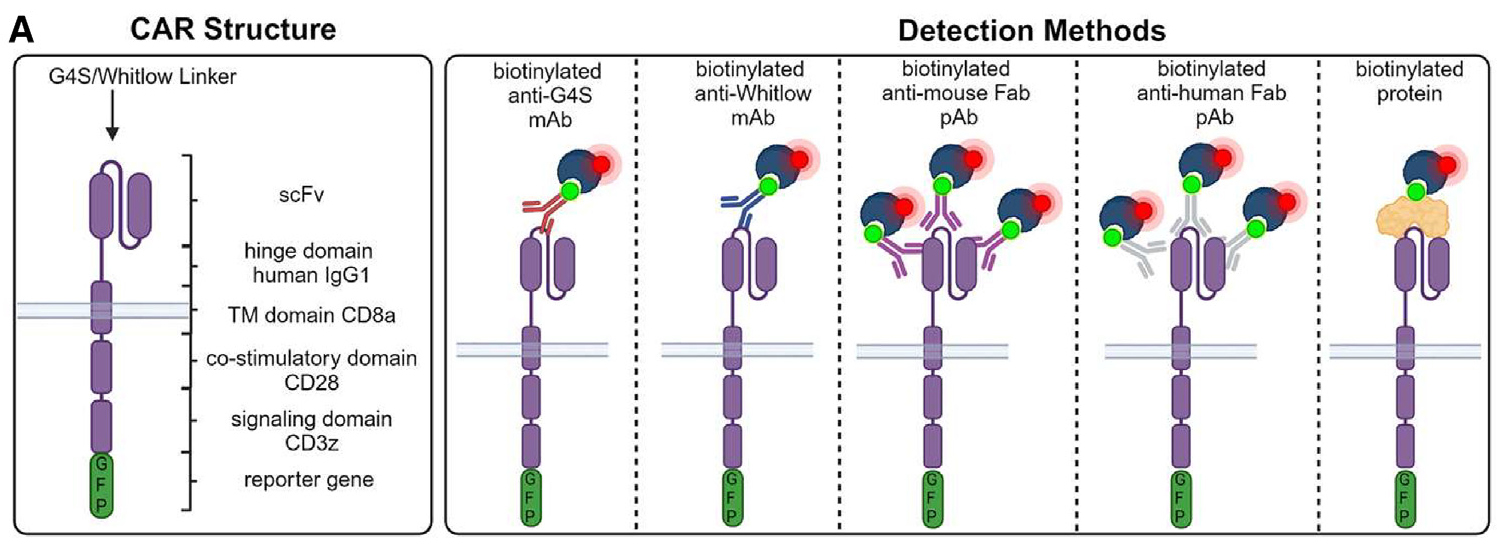
CAR不同检测技术(源自文献:doi: 10.1016/j.omtm.2024.101328)
抗连接子(linker)单抗带来了通用型CAR检测的“希望之光”。大多数CAR包含单链可变片段(scFv),Carvykti除外(具有独特的纳米抗体结构VHH)。scFv带有柔性Whitlow218或G4S连接子。连接子广泛应用于CAR构建中,标准化的氨基酸序列提供明确的靶标。不管CAR-T识别的肿瘤抗原是什么(如CD19、BCMA、Claudin18.2、CD22),只有其结构中含有连接子,抗连接子抗体均能准确的检测。与依赖scFv抗原特异性检测方法相比,抗连接子抗体显著提升检测的通用性和一致性。
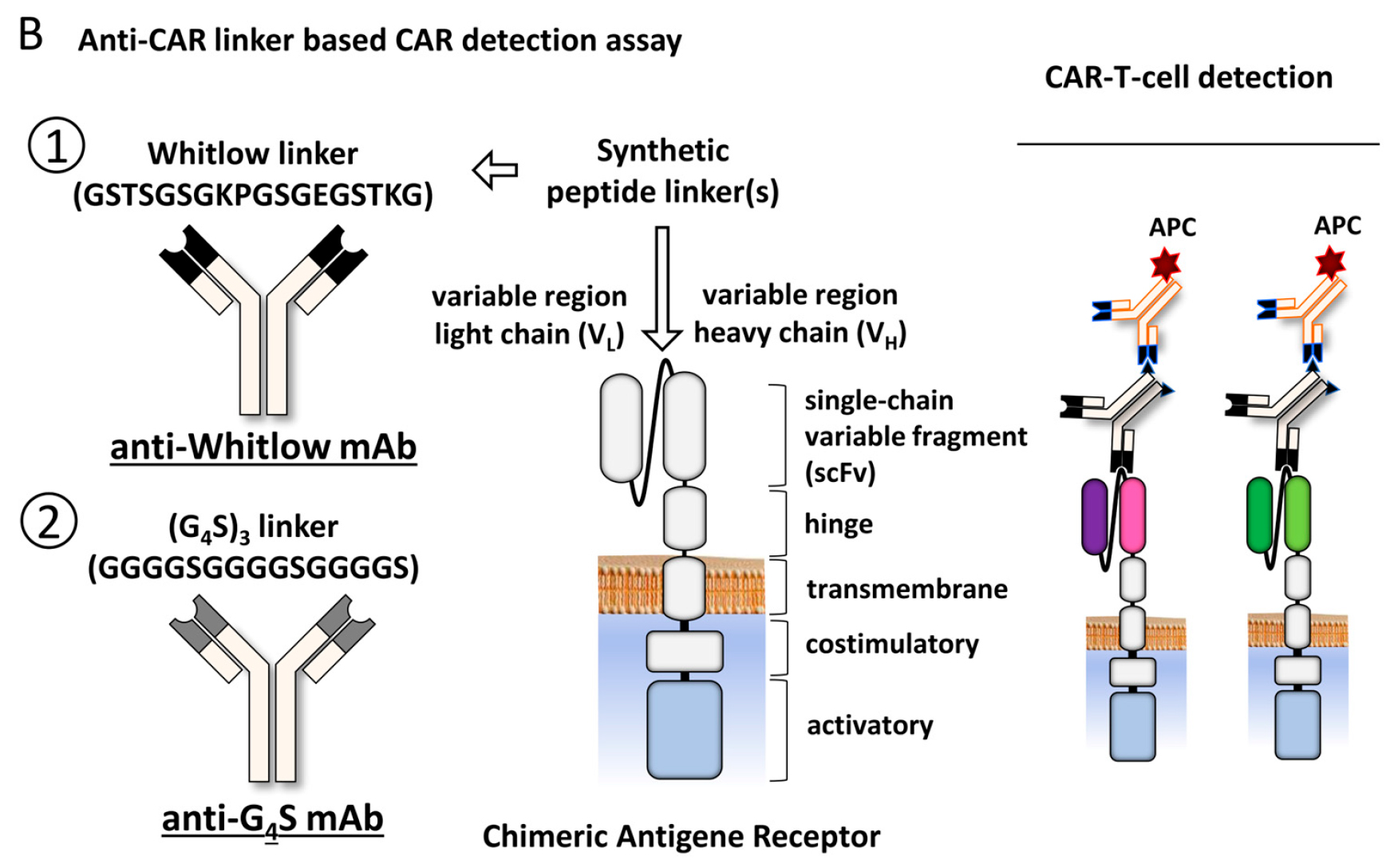
基于连接子检测CAR阳性率技术原理(源自文献:doi: 10.3390/biomedicines12081641)
抗218 Linker 抗体:高效CAR检测利器
其中218 linker具有良好的柔性和稳定性,是CAR构建中使用最广泛的连接子之一,近90%的基于scFv结构的CAR会选择这一连接子。218 linker由Whitlow等人于1993年首次报道,其氨基酸序列为GSTSGSGKPGSGEGSTKG,能促进VH和VL间的正确构象折叠,进而提高scFv的功能稳定性。
为了实现高效标准化的CAR检测,针对CAR结构中linker区域的特异性抗体逐渐火热,具有以下5大核心优势:
全场景通用:不管CAR靶向那种抗原,只有含有Whitlow218 Linker序列,就可用该类抗体进行检测,告别“一CAR一试剂”的定制化困境。
多标记选择:义翘神州抗Whitlow218 Linker抗体可以用于FITC、PE标记的流式细胞术并且APC、AF488、AF647、Biotin等标记的抗体也在开发中,即将上线。
特异性超高:自研开发的兔单克隆抗体,流式细胞术检测显示,PBMC非特异结合低于0.5%。
体内外通用:不受实验环境限制,可用于体外检测CAR-T细胞转染效率,也可在体内动态追踪CAR-T细胞扩增效果。
研发速度加快:省去定制化检测试剂的开发与验证步骤,CAR设计、表达验证周期更快速。
抗218 Linker 抗体 (验证数据:用结果说话)
高效识别CAR阳性细胞
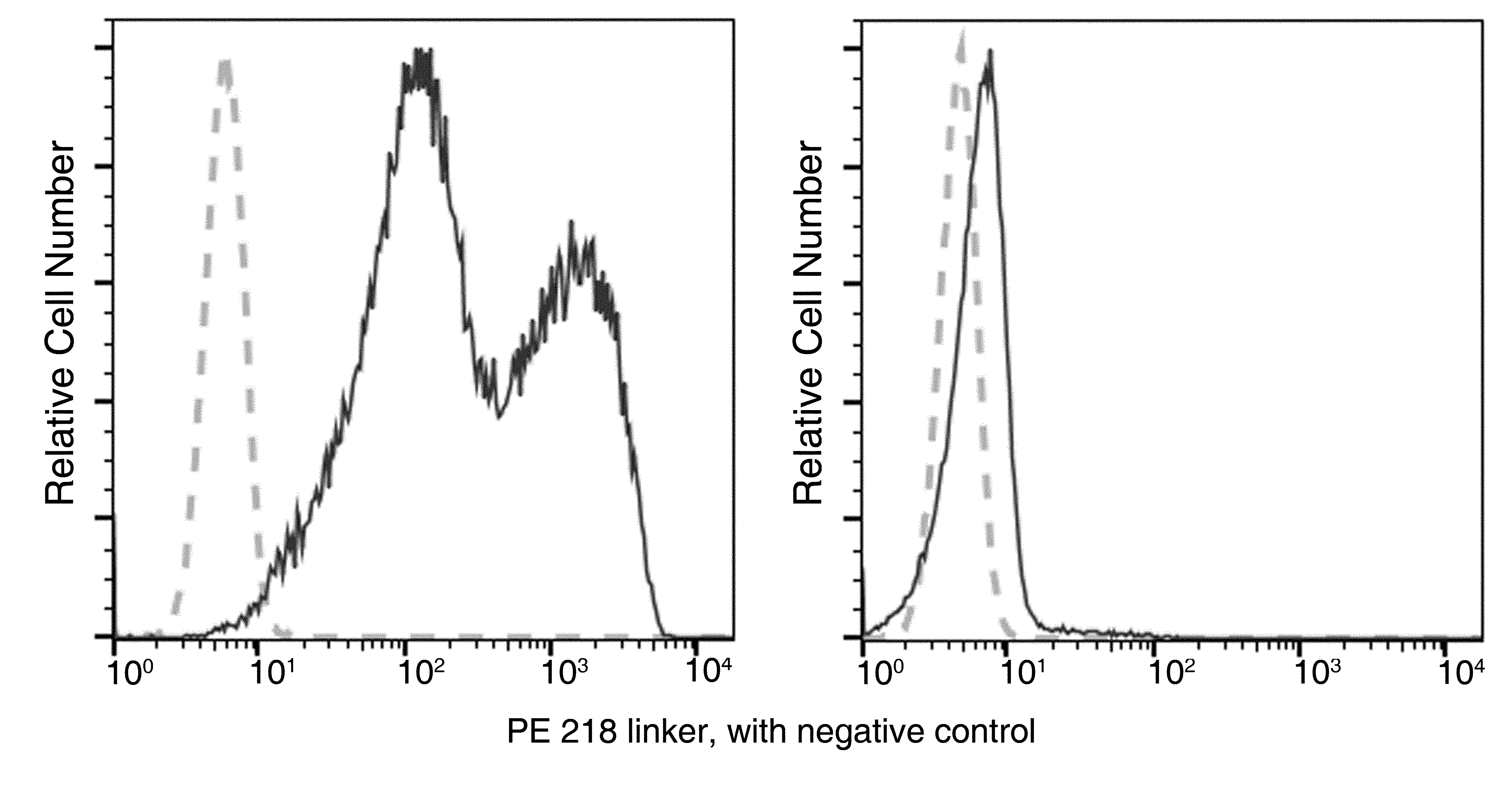
Flow cytometric analysis of anti-ERBB2 CAR expression on anti-ERBB2 CAR-transfected 293T cells. Cells were stained with PE-conjugated anti-Whitlow 218 linker Antibody (Cat: 111774-R0013-P). The fluorescence histograms were derived from gated events with the forward and side light-scatter characteristics of intact cells. Non-transduced 293 cells were used as a control (right).
高特异性结合
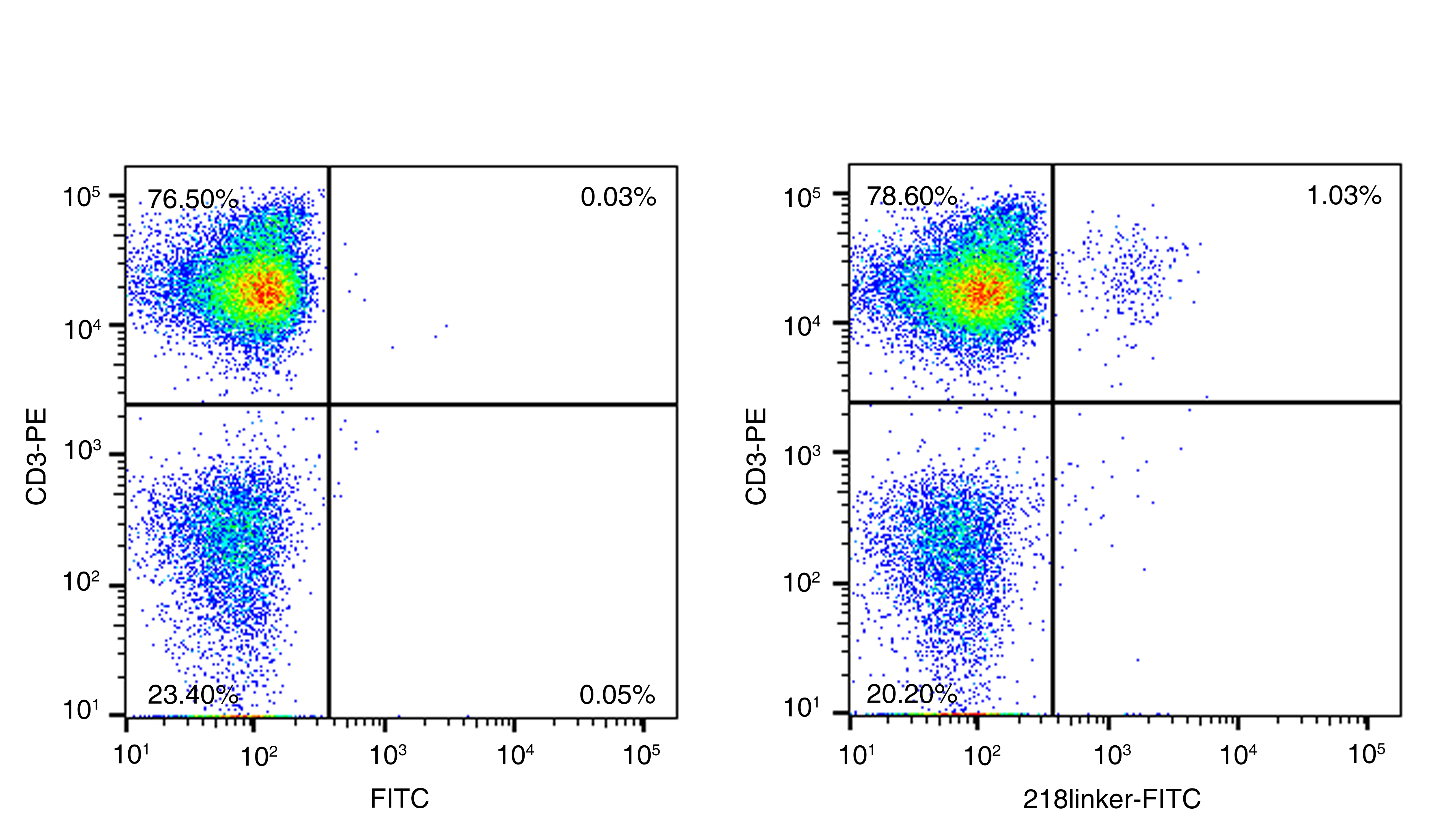
Binding activity of FITC-conjugated anti-Whitlow 218 linker Antibody to PBMC cells. PBMC cells were stained with PE conjugated anti-CD3 antibody and FITC-conjugated anti-Whitlow 218 linker Antibody (Cat: 111774-R0013-F) and detected by flow cytometry. FITC signal was used to evaluate the non-specific binding activity to PBMCs.
| 义翘神州Whitlow 218 Linker兔单抗产品 | ||
| 货号 | 标记 | 应用 |
| 111774-R0013-F | FITC | FCM |
| 111774-R0013-P | PE | FCM |
| 111774-R0013-D | AF 488 | FCM |
| 111774-R0013-G | AF 647 | FCM |
| 111774-R0013-B | Biotin | FCM |
| 111774-R0013-A | APC | FCM |
总之,抗Whitlow218 Linker兔单抗贯穿CAR-T研发全流程。临床前可快速评估CAR细胞阳率,在CMC质控中提供稳定、可重复的数据,在临床前动物模型中,动态监测CAR-T细胞的体内扩增情况。
义翘神州综合性CAR-T开发解决方案
除了抗Whitlow218 Linker兔单抗外,义翘神州还提供综合性的CAR-T细胞疗法解决方案,从CAR开发、T细胞激活、慢病毒包装、CAR-T细胞扩增到CAR-T细胞质量控制,全面支持CAR-T研究。
参考文献:
1. Katharina Schindler, et al. Linker-specific monoclonal antibodies present a simple and reliable detection method for scFv-based CAR NK cells. Molecular Therapy: Methods & Clinical Development. 2024
2. Grahnert, Aet al.Evaluation of Anti-CAR Linker mAbsfor CAR T Monitoring afterBiTEs/bsAbs and CAR T-CellPretreatment. Biomedicines 2024
3. Zhiwei Wang, et al. CAR-T therapy dilemma and innovative design strategies for next generation. Cell Death and Disease, 2025






