北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
体内CAR-T异军突起,在自身免疫性疾病方面有哪些突破呢?
1013 人阅读发布时间:2025-07-10 16:22
前言
CAR-T细胞疗法已在血液恶性肿瘤领域取得显著效果,正在扩展至实体瘤、感染性和自身免疫性疾病的临床试验。“利用免疫细胞治疗自身免疫疾病”被评为Science 2024年度十大科学突破之一。近来体内CAR-T(in vivo CAR-T)技术更是备受关注。
体内CAR-T细胞疗法已进入爆发前夜。2025年6月30日,艾伯维以21亿美元收购Capstan Therapeutics,将探索靶向CD19和BCMA的体内CAR-T疗法在自免领域的应用。其实在今年3月中旬,阿斯利康以10亿美元收购EsoBiotec时,就已经给市场带来惊喜。现在,艾伯维的直接翻倍更是让业界看到体内CAR-T发展空间。
为此,义翘神州特推出综合性的CAR-T细胞疗法开发解决方案,提供高活性靶点蛋白、细胞扩增细胞因子及无血清细胞培养基,并提供抗体发现、细胞库检定、病毒清除验证等技术服务,助力客户更方便、更快速的完成从早期靶点发现到临床前研究的多个阶段。
01 Capstan为何值21亿美元?(Science两篇、创立三年、临床一期、体内CAR-T)
2022年1月6日,宾夕法尼亚大学的Jonathan A. Epstein等人在Science发表题为:CAR T cells produced in vivo to treat cardiac injury的研究文章,开发了一种体内原位生成CAR-T细胞的新技术(in vivo CAR-T),靶向成纤维细胞激活蛋白(FAP),有助于治疗心脏纤维化疾病。
研究人员设计开发的mRNA能够表达靶向FAP的CAR,并包装到靶向CD5的脂质纳米颗粒(LNP)中,通过注射LNP递送mRNA。CD5分子在T细胞和一小部分B细胞中表达,因此可以将CAR递送至T细胞,在体内生成抗纤维化嵌合抗原受体的CAR-T细胞。体外小鼠T细胞验证,靶向CD5的LNP能将mRNA送至绝大多数T细胞中,FAP-CAR阳性表达率达到83%。人T细胞获得类似的结果。
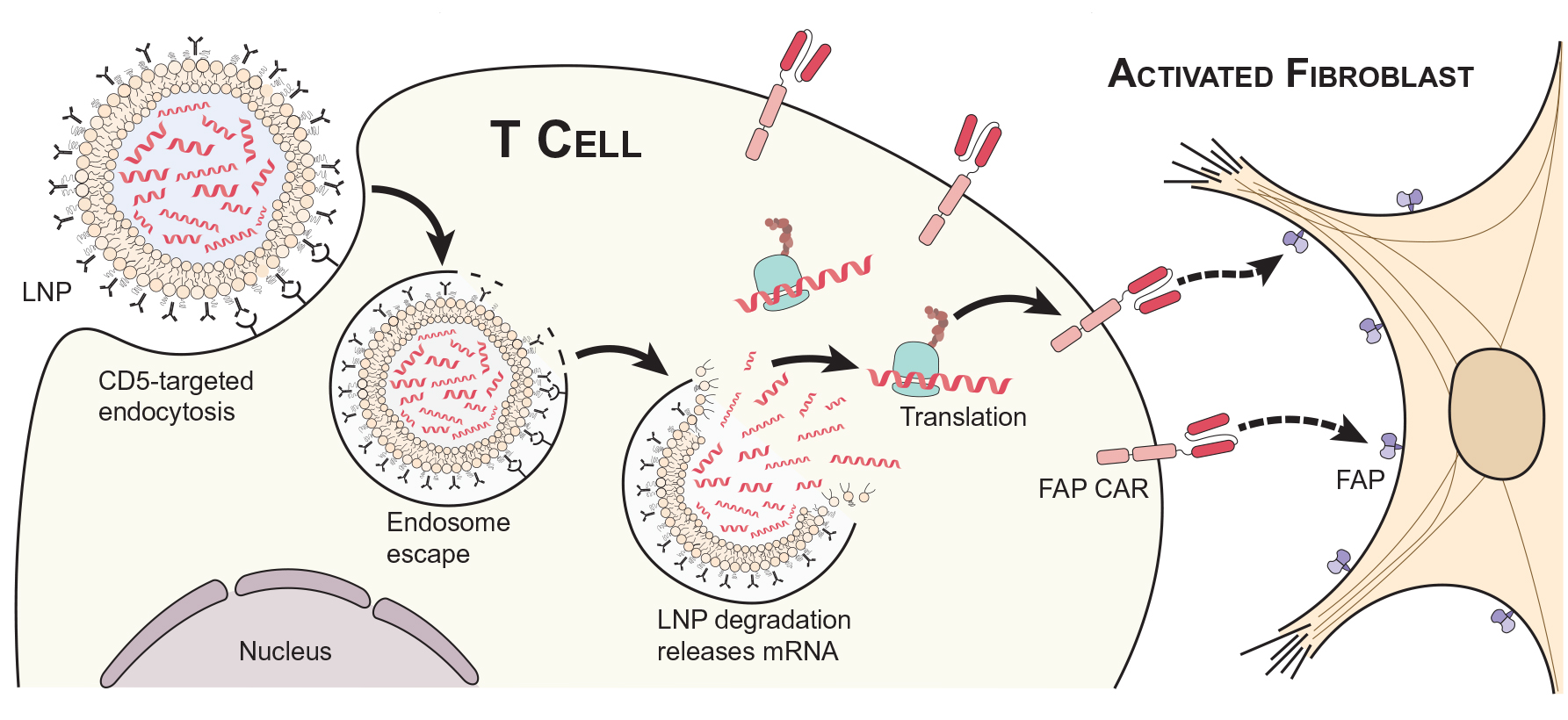
体内CAR-T技术示意图(源自文献:doi: 10.1126/science.abm0594)
不久后,Capstan Therapeutics公司成立,创始团队拥有强大阵容,包括CAR-T细胞治疗的先驱Carl June,诺奖得主、mRNA技术奠基人Drew Weissman,以及体内CAR-T技术发明人Jonathan A. Epstein,并在创始之初就获得多家制药巨头和风投机构的3.4亿美元融资。公司致力于将体内CAR-T技术应用于癌症、自身免疫性疾病及纤维化疾病的治疗。
三年后(2025年6月11日),Capstan宣布其靶向CD19的体内CAR-T疗法正式进入临床一期,用于治疗B细胞介导的自免疾病。
2025年6月19日,Capstan公司再次在Science发表题为:In vivo CAR T cell generation to treat cancer and autoimmune disease的研究文章,对体内CAR-T在啮齿类和非人灵长类动物模型中的临床前实验结果进行分析。公司专有的LNP成功将CAR mRNA靶向递送到CD8+ T细胞,对癌症和自免疾病显示出良好的治疗前景和安全性。
体内CAR-T作为一项颠覆性前沿技术,有望解决现有CAR-T疗法的痛点。目前全球获批上市的12款CAR-T均属于ex vivo CAR-T,需要将自体T细胞在体外经基因工程改造和扩增培养后,再回输到患者体内,存在生成过程复杂、周期漫长、成本昂贵等不足。
而体内CAR-T跳过体外基因改造和扩增过程,通过病毒载体、纳米载体等递送系统,直接在患者体内生成和激活CAR-T细胞。体内CAR-T能够更好地模拟体内的生理环境,让改造后的细胞更好适应并攻击靶细胞。同时,体内CAR-T能够避免体外生产过程中可能出现的细胞污染和变异风险。通过简化的治疗流程和优化的制备工艺,体内CAR-T有望降低治疗成本。
得天独厚的技术优势,吸引更多科学家和企业关注体内CAR-T。据不完全统计,全球已超过20款管线处于临床前或临床早期。国外企业有Capstan、Interius、Umoja、EsoBiotec等,国内企业有云顶新耀、济因生物、博生吉、远泰生物等。
02 CAR-T在自免领域的研究进展
最近,CAR-T细胞疗法在治疗B细胞介导的自身免疫疾病方面显示出巨大潜力。
CAR-T可以深度耗竭B细胞。B细胞耗竭不仅有利于消除产生自身抗体的浆母细胞,还可以通过废除B细胞的抗原呈递功能和细胞因子调节疾病炎症。因此,靶向B细胞的CAR-T疗法在系统性红斑狼疮、系统性硬化症、重症肌无力等疾病中展现了显著且持久的临床益处。
Theresa L. Hunter等人在食蟹猴模型中多次注射靶向CD20的CAR-T细胞导致B细胞深度耗竭。具体而言,在0.1至2.0 mg/kg的剂量范围内,三次给药后,B细胞在6小时内显著减少,且在较高剂量下(如1.5 mg/kg和2.0 mg/kg),B细胞几乎完全耗竭。恢复的B细胞主要为初始表型,表明发生了免疫重置。
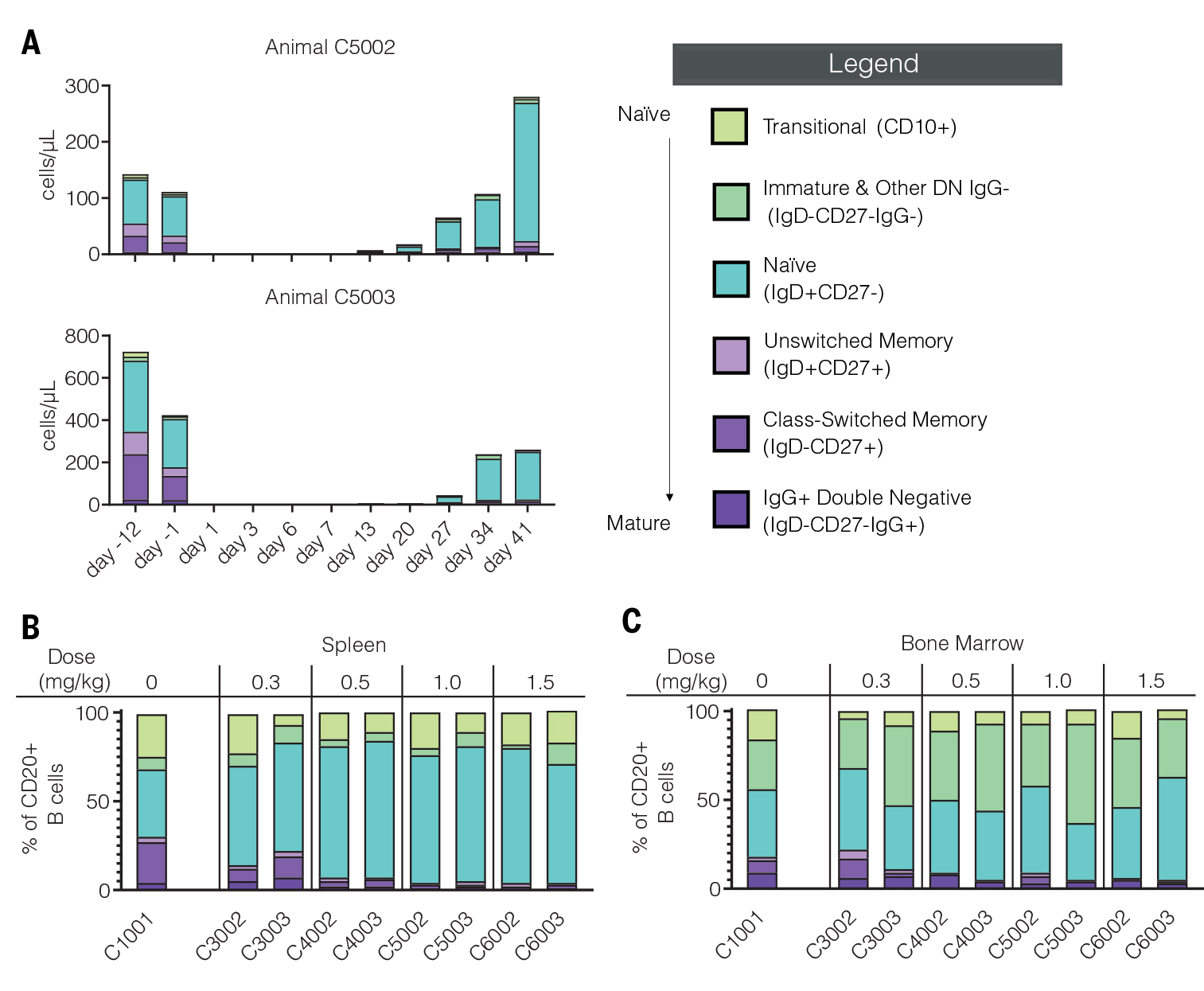
体内CAR-T治疗导致B细胞深度耗竭并发生免疫重置(源自文献:doi: 10.1126/science.ads8473)
CAR-T靶点选择同样重要。现在大多数针对自免疾病的CAR-T靶向CD19和BCMA。CD19对B细胞谱系具有高度特异性,在整个B细胞分化途径中表达。BCMA在成熟B细胞群中优先表达,包括记忆B细胞、浆母细胞和浆细胞,可能更具优势。
CD38也是CAR-T值得关注的靶点,在浆细胞、早期B细胞、T细胞亚群和NK细胞上表达,可提供不同的靶细胞谱。靶向CD38不影响成熟B细胞,而靶向抗体产生的细胞,在清除早期分化阶段的B细胞方面有优势。
对于银屑病、炎症性肠病、脊柱关节炎等由异常T细胞激活和IL-23、IL-17介导的炎症导致的自免疾病,CAR-T难以作出响应,可能需要更合适的细胞疗法,比如Treg细胞或间充质干细胞移植。
评估CAR-T细胞疗法的效果,不仅取决于疾病的生理学机制,还取决于是否存在可测量且可靠的临床重点。如多发性硬化症患者需要数年时间才能证明疾病发作减少或消失,长时间的研究颇具挑战性。
总之,CAR-T从肿瘤领域“跨界”来的自免疾病领域,正在改写其治疗规则。开发更多靶点或双靶点组合,覆盖更广的B细胞谱系能够减少CAR-T的脱靶风险,提高安全性和有效性。
义翘神州综合性CAR-T开发解决方案
作为一家专注于为全球生物医药领域提供关键试剂和技术服务的高新技术企业,义翘神州特地推出了综合性的CAR-T细胞疗法开发解决方案,多方位地支持客户更方便、更快速地完成从早期靶点发现到临床前研究的每一个阶段。
【参考文献】
1.Joel G. Rurik, et al. CAR T cells produced in vivo to treat cardiac injury. Science, 2022. doi/10.1126/science.abm0594
2.Theresa L. Hunter, et al. In vivo CAR T cell generation to treat cancer and autoimmune disease. Science, 2025. doi/10.1126/science.ads8473
3. Schett, G. et al. Advancements and challenges in CAR T cell therapy in autoimmune diseases. Nat Rev Rheumatol 2024.






