北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
3分钟了解ELISPOT技术检测B细胞免疫应答的5大关键步骤
53 人阅读发布时间:2026-03-26 16:13
B细胞是免疫系统中的“主角”,通过识别抗原、产生抗体及记忆免疫等,为人体提供有效的免疫防御。免疫记忆是疫苗发挥保护作用的基础。
在人类与传染病病毒战斗的漫长历史中,疫苗无疑是优秀的发明之一。但是,为什么有些疫苗能够提供终身保护而有些需要打“加强针”呢?这与特异性、长寿命记忆B细胞密切相关。
B细胞免疫应答和抗原特异性抗体IgM、IgA和IgG的产生对治疗疾病和预防病毒再次感染至关重要。病毒感染或接种疫苗后产生的功能性中和抗体有利于病毒清除,并且可以通过体外实验进行定量分析,是接种疫苗后成功建立免疫应答的标志。
体内具有免疫功能的B细胞有两种存在形式:激活状态和静息状态。一般疫苗接种3-9天内会存在激活状态的B细胞。免疫组化、流式细胞术、单细胞测序、抗体检测等用于B细胞研究。ELISPOT具有灵敏度高、准确性好、能够在单细胞水平上检测和定量等优势,已广泛应用于T细胞和B细胞的功能性检测中。
本文我们将以SARS-CoV-2病毒mRNA疫苗研究为例,详细介绍ELISPOT技术在定量检测特异性记忆B细胞频率领域的实验设计思路及操作步骤。
免疫应答产生的抗体和记忆B细胞(MBCs)是病毒免疫记忆的重要组成部分。刺突蛋白是B细胞产生中和或保护性抗体的主要靶点。Kennedy等人开发了一种检测记忆B细胞的ELISPOT技术,用于检测新冠病毒感染和/或疫苗接种后特异性B细胞的频率。该技术成功用于SARS-CoV-2病毒mRNA疫苗接种后记忆免疫应答的动态特征研究,以及评估疫苗诱导的MBCs对病毒突变株的交叉反应性。结果发现,在mRNA疫苗接种过程中,抗原特异性记忆B细胞的频率随时间发生显著变化/升高,且受试者间存在较大差异。
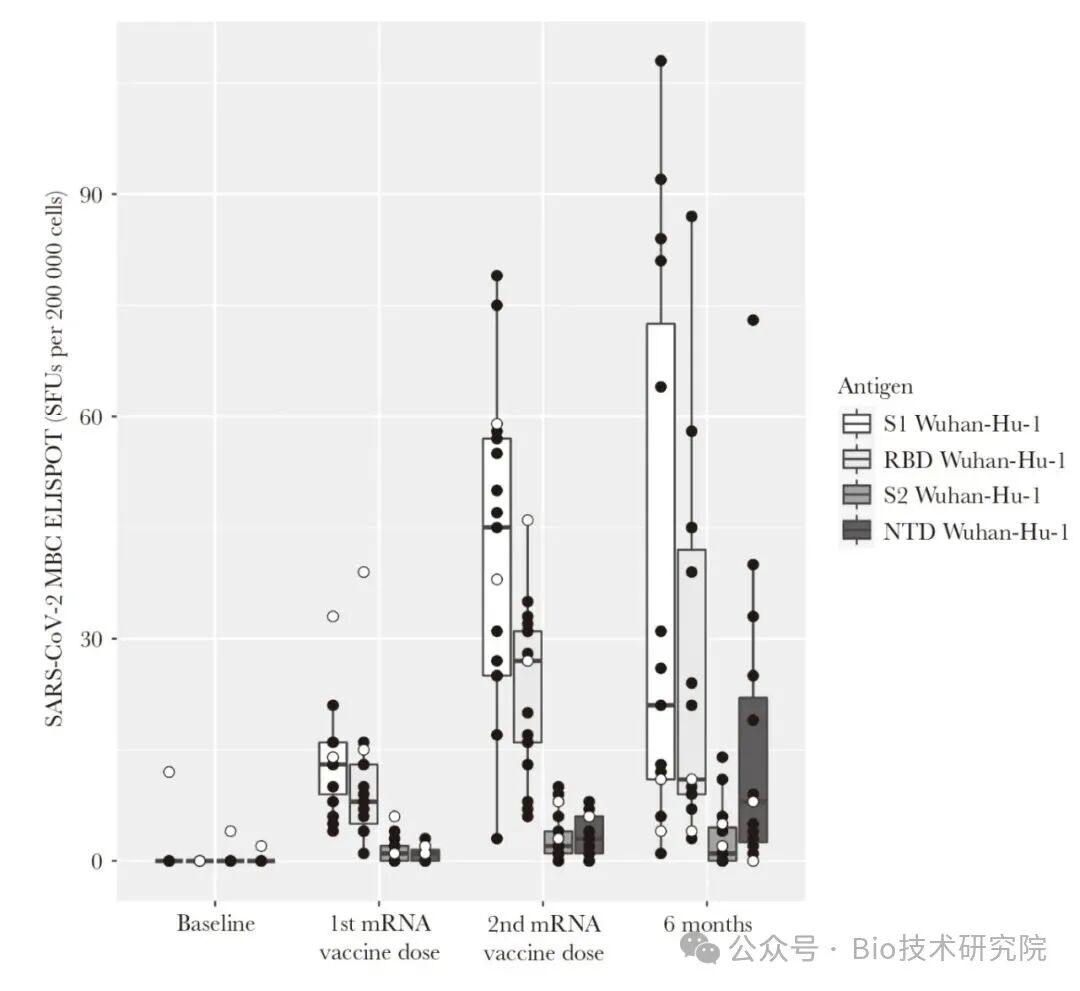
利用ELISPOT技术检测B细胞免疫应答在接种疫苗后的动态变化
实验操作步骤
1. 外周血单个核细胞(PBMC)的采集、分离、冻存
本次实验采用Ficoll密度梯度离心法收集接种疫苗人群的PBMC,详细操作步骤可参考“解决PBMC制备难题,手把手教你Ficoll离心,让免疫学实验数据登上顶刊”一文。
2. PBMC细胞复苏
实验检测SARS-CoV-2抗原特异性IgG MBC的ELISPOT方案使用低温保存的PBMC,因此需要先将冻存细胞进行复苏。如果实验条件允许,建议使用新鲜分离的PBMC。
2.1 在RPMI培养基中添加DNA酶,37℃水浴中至少预热15min。
2.2 在15mL的离心管中加入100μL预热的RPMI培养基。
2.3 从液氮罐中取出PBMC(细胞浓度1×107 Cells/mL),将其快速置于37℃水浴中,直至剩余少量冰。
2.4 迅速用70%乙醇擦拭冻存管,用移液器将冻存管中的PBMC移至含有RPMI培养基的离心管中。轻轻摇晃混匀。随后缓慢加入500μL预热的RPMI培养基。此步骤需在无菌条件下操作。
2.5 每隔1min向离心管中加入1mL的培养基,直至细胞悬液体积达到10mL。盖紧瓶盖,颠倒混匀5次,不要涡旋细胞悬液。
2.6 25℃下300×g离心7min,离心机加速刹车开启。
2.7 移除上清液,加入10mL培养基重悬细胞,颠倒混匀5次。
2.8 将离心管置于37℃水浴中,孵育细胞20min。每隔10min颠倒一次离心管。孵育结束后将离心管置于冰上7min。
2.9 4℃下300×g离心7min,离心机加速刹车开启。
2.10 小心移除上清,用1mL添加5%胎牛血清的RPMI培养基重悬细胞。
2.11 取新的50mL无菌离心管,将细胞过滤网置于离心管顶部。通过滤网,将细胞悬液从15mL离心中移至50mL离心管中。
2.12细胞计数:取12.5μL细胞悬液,加入200μL 1×PBS、37.5μL台盼蓝,充分混匀。取10μL样品进行细胞计数。
2.13 通过添加含有5%胎牛血清的RPMI培养基,将细胞浓度调整至2×106 Cells/mL。
3. B细胞预刺激
ELISPOT实验定量检测MBC频率,需要在体外非特异性预刺激B细胞。本次实验选用Toll样受体(TLR)激动剂R848和重组人白细胞介素(IL)-2(rhIL-2)联合刺激。
3.1 在24孔无菌细胞培养板,每孔中加入2mL PBMC悬液(浓度为2×106 Cells/mL),使每孔含有4×106个细胞。
3.2 每孔加入20μL rhIL-2,终浓度为10ng/mL。然后向每孔加入2μL R848,使其终浓度达到1μg/mL。
3.3 37℃、5% CO2培养箱中,孵育细胞72h。
4. ELISOPT板包被
抗原包被应在预刺激实验的第二天进行。
4.1 用磷酸盐缓冲液(PBS, pH 7.4)将SARS-CoV-2重组蛋白稀释至2μg/mL,将抗人总IgG捕获单克隆抗体(mAb MT91/145)稀释至15μg/mL。
4.2 PVDF膜在包被前需用乙醇活化。如Millipore公司的PVDF板应每孔加入50μL 70%乙醇处理,最长2分钟。乙醇处理后立即用PBS洗板,重复5次。
4.3 根据实验设计,在对应的孔中加入100μL 稀释后的重组蛋白,确保每种抗原的特异性检测至少设置4个复孔。设置对照孔,仅用100μL pH 7.4的PBS包被,作为阴性对照。设置总抗体IgG包被孔,每孔加入100μL 抗人总IgG捕获单克隆抗体。
4.4 用膜密封96孔板,4℃孵育过夜。
5. B细胞ELISPOT实验设置
5.1 预刺激步骤完成后,将同一受试者的所有培养基/细胞合并至一个15 mL离心管中(若细胞量较多,则使用50 mL离心管)。
5.2 细胞培养孔底或壁上可能黏附细胞,需向每孔中加入0.5mL预热的0.25%胰蛋白酶-EDTA。并置于37℃、5% CO2培养箱中10min,直至细胞脱落。
5.3 将每孔细胞-胰蛋白酶悬液移入相同样本对应的离心管中。
5.4 重复步骤5.2-5.3一次。
5.5 向每孔中加入0.5mL含有5%胎牛血清的RPMI培养基,上下吹打均匀。将每孔悬液移入相同样本对应的离心管中。
5.6 向每个离心管中添加含有5%胎牛血清的RPMI培养基,将其体积补足至10 mL。
5.7 4℃下300×g离心7min,离心机加速刹车开启。
5.8 在不扰动细胞沉淀的情况下移除上清液。然后用0.5mL含有5%胎牛血清的RPMI培养基重悬细胞。将细胞置于冰上。
5.9 每个样本取12.5μL细胞悬液进行细胞计数。并用含有5%胎牛血清的RPMI培养基,将细胞浓度调整至2×106 Cells/mL。
5.10 提前一小时将预包被的ELISPOT板从4℃取出,进行封闭。
5.11 封闭:先弃去包被试剂,每孔加250μL无菌PBS,洗剂5次。每孔加200μL封闭液(添加10%胎牛血清的RPMI培养基)。在生物安全柜中室温孵育1h。
5.12 移除封闭液,将板在纸巾上拍干,直至ELISPOT板中无培养基残留(在生物安全柜中操作)。
5.13 每孔加100μL细胞悬液(浓度2×106 Cells/mL),分别加入SARS-CoV-2 抗原包被孔和空白(无抗原)细胞对照孔中。
5.14 向100μL细胞悬液中加入900μL培养基,对细胞悬液额外进行1:10稀释。取50μL稀释后的细胞悬液(每孔1万个细胞)加入总IgG包被孔(例如每位受试者4个孔),再向总IgG包被孔中加入50μL含5%胎牛血清的RPMI培养基,使每孔总体积达到100μL。
5.15 用铝箔覆盖板,37℃、5% CO2培养箱中,孵育细胞24h。孵育期间不要扰动细胞。
6. 记忆B细胞频率测定
6.1 低渗裂解细胞:从培养箱中取出ELISpot板,弃掉孔内液体,在滤纸上拍干。然后在每孔中加入200μL 4°C预冷的去离子水,置于4°C冰箱10min。
6.2 洗板:完成裂解后,弃掉孔内液体并拍干。接着每孔中加入200μL无菌的PBS,浸泡1min。然后弃掉孔内液体,拍干。重复洗板操作5次。
6.3 检测抗体孵育:每孔加入100μL稀释好的检测抗体,室温条件下孵育2h。
6.4 洗板:抗体孵育结束后,弃掉孔内液体并拍干。然后向每孔中加入200μL无菌的PBS进行洗板。重复洗板5次。
6.5 Streptavidin-ALP孵育:每孔加入100μL稀释好的Streptavidin-ALP,室温条件下孵育1h。
6.6 洗板:抗体孵育结束后,弃掉孔内液体并拍干。然后向每孔中加入200μL无菌的PBS进行洗板。重复洗板5次。
6.7 显色:每孔加入100μL底物显色液,室温避光孵育5-30 min,根据斑点生成情况选择终止显色时间。
Tips:显色反应通常发生在10-30 min,通过目视监测斑点的形成过程。
6.8 终止反应:待斑点出现后,用大量自来水或去离子水冲洗。建议揭开板底座,冲洗膜的底部。
6.9 读数:将ELISpot板放置在室温阴凉处,待板完全干燥后再进行读数。可使用斑点分析仪或显微镜进行斑点计数及分析。
Tips:请勿在高于37°C的温度下干燥膜板,否则可能导致膜破裂。斑点计数时,应注意区分由纤维、膜撕裂、碎片等导致的不规则斑点,一般细胞生成的斑点通常为圆形。






