北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
解决PBMC制备难题,手把手教你Ficoll离心,让免疫学实验数据登上顶刊
266 人阅读发布时间:2026-03-26 15:56
免疫学实验技术越来越精准,如ELISpot能够捕捉单细胞水平的细胞因子分泌状态,超高灵敏度,检测百万分之一的细胞。然而,再先进的技术也需要高质量的研究对象。
外周血单个核细胞(PBMC)的质量,直接决定了你的ELISpot、流式细胞数据是发表在顶刊还是“水刊”。
接下来我们将用3000多字的深度拆解,带你攻克PBMC制备的技术“暗礁”!内容主要包含以下几个方面:PBMC免疫学研究基础、Ficoll密度梯度离心步骤、PBMC冻存和复苏、PBMC提取细节、专属ELISpot的优化细节
一、PBMC:免疫学研究的基础
外周血单个核细胞(PBMC,Peripheral Blood Mononuclear Cells)是免疫学研究中最常用的样本之一,常作为WB、ELISA、ELISpot、流式细胞术等实验的研究对象。PBMC的特征是有一个圆形的细胞核,包括:
1. 淋巴细胞(约占PBMC的95%):T细胞(70%)、B细胞(15%)、NK细胞(10%)
2. 单核细胞(5%):分化为巨噬细胞和树突状细胞
3. 树突状细胞(1%):功能强大的抗原呈递细胞
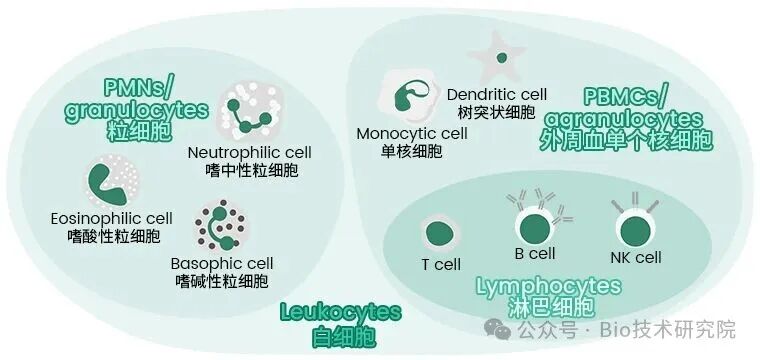
这些细胞不仅是ELISpot检测的核心对象,更是WB、流式细胞术等实验的常客。与组织来源的细胞不同,PBMC的获取无需杀死实验动物,仅需一管外周血即可开展研究,因此在人类免疫学研究、疫苗评价、肿瘤免疫治疗等领域具有不可替代的地位。
关键认知:PBMC的质量不是“有就行”,而是“好才行”。Dead cell=Dead data,这一公式应刻在每个免疫学研究者的心中。
二、Ficoll密度梯度离心:制备PBMC的"黄金标准"
PBMC是外周血中的重要细胞群体,能够代表外周血的免疫状态,是研究免疫系统、疾病机制和开发免疫疗法的重要工具。PBMC来自全血,常用蔗糖聚合物(Ficoll)密度梯度离心法制备,操作步骤如下:
1,实验前准备:Ficoll密度梯度介质提前恢复至室温(18-20℃)。
2,1:1稀释全血:将抗凝全血从采血管转移至新的无菌50 mL离心管中,加入等体积的PBS。轻轻颠倒管子,使血液和PBS混匀。
3,准备离心:取新的50 mL离心管,先加入15 mL Ficoll,再加入稀释后的15 mL血液。血液要缓慢的加入,可适当倾斜离心管,使移液器枪头紧靠管壁,位于Ficoll液面上5-10mm处,慢慢加入,避免Ficoll分离介质和血液界面搅乱,保持两种液体分界面清晰。
4,密度梯度离心:将离心管放入离心机,室温1000 x g离心30min。请注意:要关闭离心机的快升速和减速设置,防止升速或降速过快破坏液体分层。
5,收集PBMC:用移液器缓慢吸掉上层血浆层(约15mL)。然后从边缘开始,缓慢吸取PBMC层至新的离心管中。剩余的Ficoll和红细胞层可弃掉。
6,洗涤:在PBMC中加入5倍体积的PBS或培养基,室温300x g离心5-10min。小心弃去上清。为确保Ficoll彻底清除可重复洗涤一次。
7,重悬细胞:加入5-10mL培养基,轻柔吹打,重悬细胞。
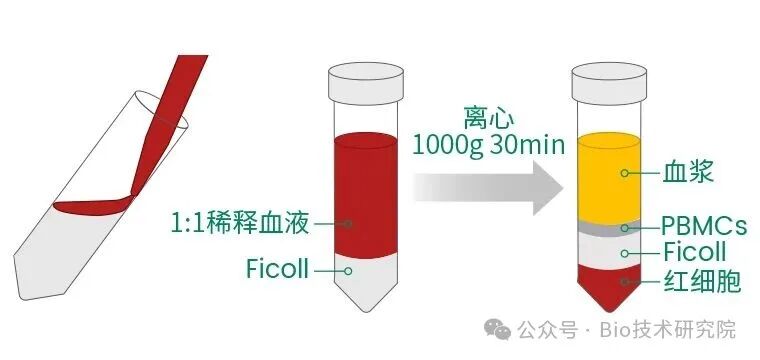
Ficoll密度梯度离心的核心原理是利用细胞密度的差异来进行物理分层。PBMC的体积、形态和密度与外周血其他细胞不同。Ficoll是蔗糖的多聚体,中性,不会穿过生物膜,可用于PBMC的分离液。Ficoll是通过特定的调整,密度保持在1.077 ± 0.001 g/mL。
如上图所示,红细胞、粒细胞密度大,离心后沉于管底。淋巴细胞、单核细胞密度小于Ficoll的密度,离心后漂浮于其上。Ficoll处于PBMCs与不需要的粒细胞和红细胞层之间,起到隔离的作用。因此吸取白膜层细胞,并进行合适的洗涤,就可从外周血中分离获得较高纯度的PBMC。
|
细胞类型 |
近似密度(g/mL) |
|
血小板 |
~1.03 |
|
PBMC |
~1.07 |
|
红细胞、多核细胞 |
~1.08 |
|
Ficoll |
1.077±0.001 |
温度是“隐形杀手”。Ficoll的密度会随温度波动,最佳温度是室温(18-20℃)。室温条件下,红细胞与Ficoll有效聚集。温度过高会使PBMC中混入Ficoll,降低PBMC回收率。温度过低则会阻碍红细胞和粒细胞渗透到密度较高的Ficoll中,造成PBMC污染。因此,Ficoll密度梯度离心应在室温下进行。切记:离心机温度设为20℃,千万不要用4℃!
三、冻存与复苏:让时间停止的生物技术
关于PBMC的冻存和复苏,可参考上一篇文章:《实操干货 | 小鼠脾细胞制备、冻存、复苏全流程详解》,这里我们不再赘述。
关键是做到“慢冻快融”!
冻存最佳降温速率为1℃/min,这能让细胞在冰晶形成和渗透压变化中找到生存平衡点。-80℃不是终点!细胞在此温度下仍有微弱代谢,长期储存会导致功能丧失。必须在24小时内转入液氮。
复苏后细胞常因DNA释放而聚团。在培养基中加入SuperNuclease®等核酸酶,可有效解离细胞团块,提高回收率,且不影响ELISpot结果。
四、细节是PBMC成功的关键
静脉穿刺是常用的采血方法,在操作时要采用一些适当的防护措施。
要想获得单个核细胞悬液,需对全血进行抗凝处理。3种常用的抗凝剂有EDTA、肝素、柠檬酸盐。研究已经证实,这3种抗凝剂均适用于PBMC制备,且在ELISpot检测中结果相近。采血与PBMC分离之间的时间间隔会显著影响ELISpot实验结果。有两个研究团队提供的证据表明,为获得最佳的ELISpot反应,需在采血后8小时内完成PBMC分离。而早在20世纪80年代就已有文献报道延迟血液处理所带来的负面影响。
建议使用新鲜血液样本,抽血后全血样本室温放置不宜超过5-8小时,不要冷藏。如需运输,样本应在环境温度下运送到所需的实验室。
血液样本储存超过20小时,PBMC可能会被活化的粒细胞污染。这将导致T细胞反应显着降低。防止这种污染的方法:
1. 在常温储存前,用PBS或RPMI-1640培养基1:1稀释血液样本;
2. 抽血后耗尽粒细胞;
轻轻混合血液样本,直到PBMC分离。
成功分离PBMC依赖于多种因素。其中在试管中加入蔗糖聚合物Ficoll时,不能与血液混合。可以如图所示提前加入Ficoll,如果是将Ficoll铺在血液上层,需要缓慢小心的移动液体。目前有预填充Ficoll(位于隔层下方)的多孔硬质隔层试管(如Leucosep或Accuspin试管),更方便这一步的操作。当获取血液后,可快速且轻松的将其加入试管,无需担心血液与Ficoll发生混合。与传统分层法相比,该方法能节省大量时间,且PBMC得率与传统方法相当。
五、专属ELISpot的优化细节
核心问题在于:究竟是什么原因导致ELISpot检测结果下降?研究发现主要原因是粒细胞,它们会在采血后被激活。接下来我们将详细讨论一下相关的机制:
粒细胞被激活后其密度会发生改变,无法通过Ficoll密度梯度离心将其从PBMC中分离。因此相当于对PBMC进行了稀释,而斑点数的减少与粒细胞污染程度正相关,比如20%粒细胞污染=少加20% PBMC=少20%斑点。粒细胞在冷冻和解冻过程中会有大量死亡,出现细胞聚集效应,进一步影响ELISpot结果。
当粒细胞被接种到ELISpot板中时,还会通过自身Fc受体与捕获抗体的Fc段结合,粘附在膜上,对斑点造成物理性破坏。
粒细胞在采血后被激活,会释放过氧化氢,促使精氨酸酶激活,进而导致CD3 zeta链表达下调,干扰T细胞受体(TCR)的信号转导。这种机制是导致血液处理延迟后,在ELISpot检测结果中观察到T细胞功能受到抑制的根本原因。
那么有没有办法既能避免粒细胞污染又能减少其激活带来的影响呢?
关键的操作就是采血后快速分离PBMC。若在采血几小时后完成PBMC分离,可将粒细胞污染及其激活带来的影响控制在可控范围内。
McKenna及其同事深入研究了采血后不同处理场景下粒细胞的污染情况。
他们对同一个供体的不同管血液进行处理,结果显示,室温储存8小时后,PBMC中粒细胞的污染程度是采血后立即分离PBMC的两倍。
而室温储存24小时后再分离PBMC,其粒细胞污染会增加近10倍,若在4℃储存24小时,其污染会增加近100倍。
但是采血后立即用PBS或RPMI培养基将血液按1:1稀释,室温储存24小时,粒细胞污染程度会降低,与血液在室温储存8小时效果相当。血液稀释能降低粒细胞的激活,
因此,无法在8小时内完成PBMC分离可在无菌条件下对血液进行稀释。例如将血液稀释到预装PBS的50mL试管中,在室温下运输到实验室再进行后续的PBMC分离。该方法已获得国际糖尿病免疫学会(IDS)T细胞研讨会委员会的推荐。
总之,PBMC的制备融合了生物物理学、细胞生物学和免疫学多种精细技术。从抗凝剂选择到Ficoll铺层手法,从8小时黄金窗口到“慢冻快融”的温度控制,每个细节都在为你的ELISpot数据投票。
高质量的PBMC样本是免疫学实验(尤其是ELISpot)成功的一半。当我们在面对惨淡的实验结果时,追溯到细胞制备的第一步,也行问题就藏在那个还没来得及换的枪头里。






