北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
以病毒生命周期为核心,抗病毒药物开发面临的挑战与策略
151 人阅读发布时间:2025-11-19 16:17
病毒,结构简单却极具感染性的病原体,对全球公共卫生安全造成重大挑战。从流感大流行,到近年来的SARS、MERS、埃博拉、基孔肯雅热等,无不警示着人类与病毒斗争的持久性和复杂性。
抗病毒药物是对抗病毒感染的重要策略之一,是医学界和制药行业关注的焦点之一。抗病毒药物主要通过干扰病毒生命周期的某个阶段,如吸附、入侵、脱壳、复制、释放等,来阻止病毒的复制与传播。
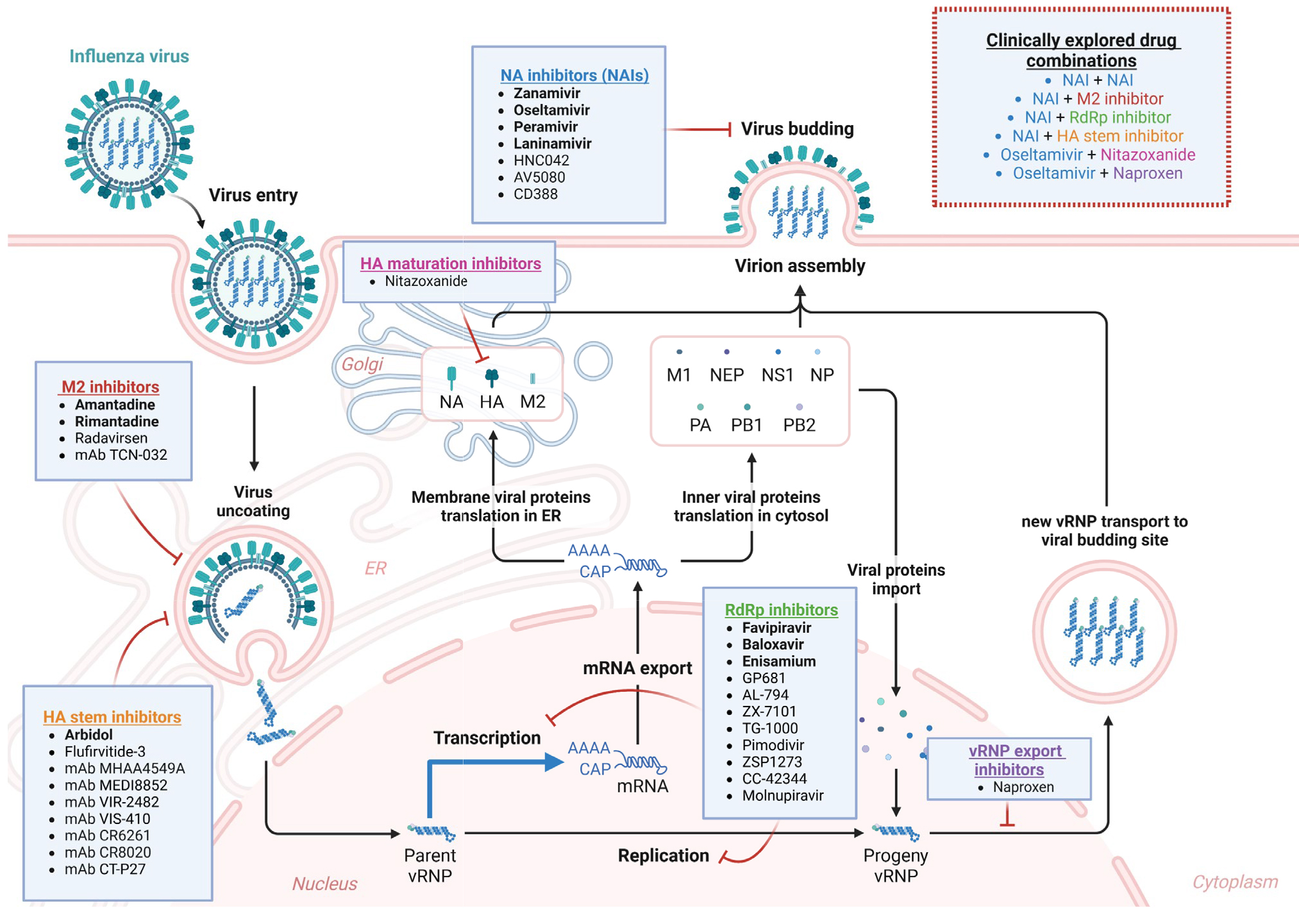
针对流感病毒生命周期开发抗病毒药物策略(源自文献:doi: 10.1007/s00018-025-05611-1)
抗病毒药物的分类与作用机制
根据抗病毒药物的作用机制和靶点不同,可分为以下几类:
01 核苷酸类似物
通过模拟天然核苷酸的结构,以假乱真,导致病毒复制过程提前终止或产生无功能的病毒基因组,进而抑制病毒复制。如Remdesivir作为一种广谱抗病毒药物,其活性代谢产物可抑制RNA依赖性RNA聚合酶(RdRp),阻止核糖核蛋白(RNP)的合成。
02 蛋白酶抑制剂
通过与病毒特定酶的变构位点结合,改变酶的构象,从而抑制其活性。2025年11月5日,国家药品监督管理局(NMPA)获批的奥格特韦(Olgotrelvir)以SARS-CoV-2关键蛋白水解酶(Mpro)和宿主组织蛋白酶L(CTSL)为靶点,阻止病毒复制及降解病毒刺突蛋白,双重机制抑制病毒入侵。奥司他韦(Oseltamivir)则是流感病毒神经氨酸酶抑制剂,通过阻止病毒从感染细胞释放,抑制病毒扩散。
03 整合酶抑制剂
通过阻断病毒整合酶的活性,防止病毒DNA整合到宿主细胞基因组中,从而中断病毒复制周期。以HIV治疗为例,2007年第一个整合酶抑制剂在美国上市,自此HIV治疗进入整合酶抑制剂时代。
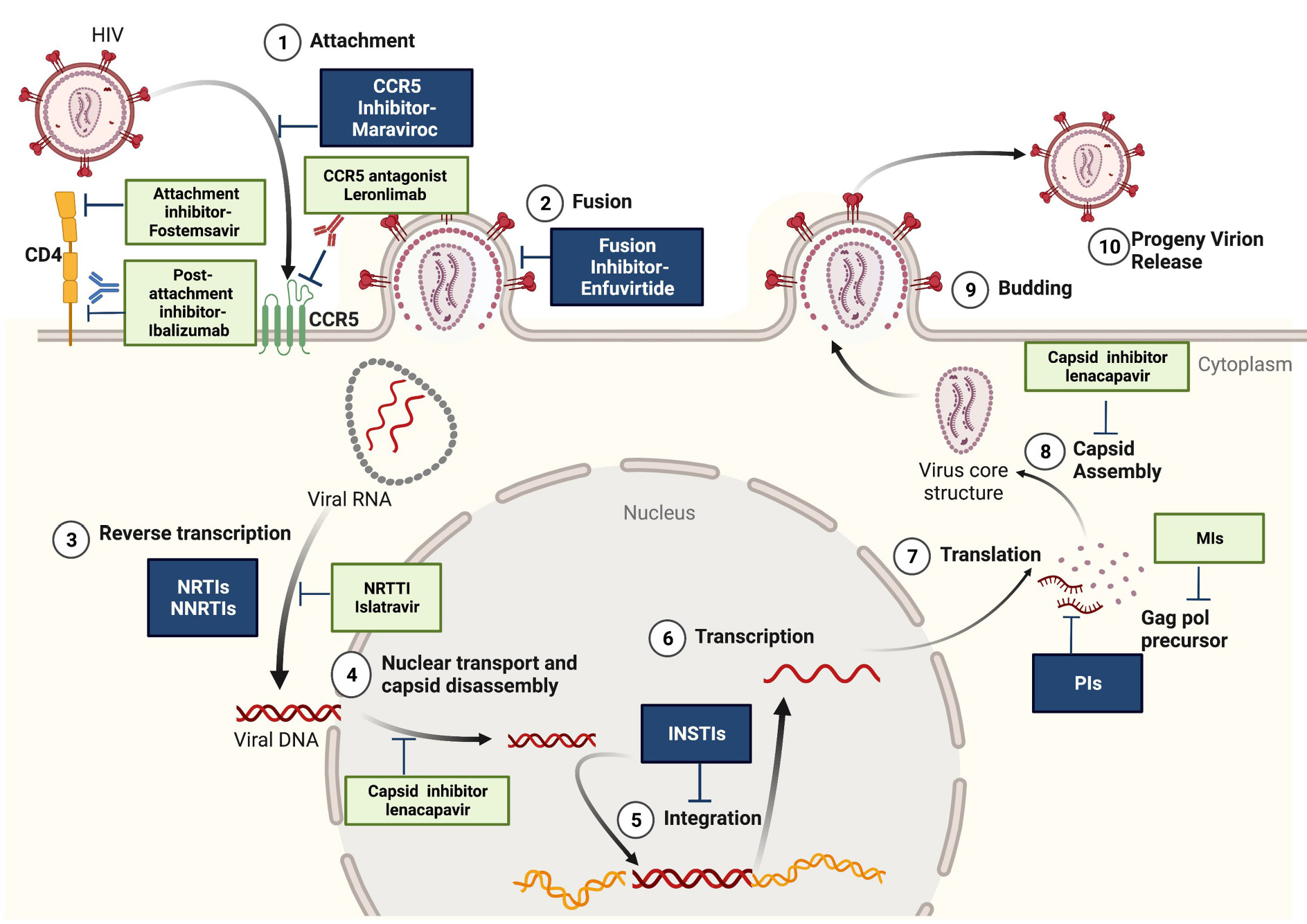
针对HIV生命周期开发抗病毒药物策略(源自文献:Doi: 10.3389/fmicb.2023.1133407)
04 免疫调节剂
如干扰素,通过激活宿主细胞的抗病毒状态,增强免疫系统对病毒感染细胞的识别和清除能力。
靶向病毒生命周期关键步骤的研发策略越来越精细化。如靶向病毒刺突蛋白或宿主受体(ACE2)的抑制剂或抗体可以阻止病毒吸附和侵入,RdRp抑制剂阻止病毒基因组的复制与转录,蛋白酶抑制剂阻止蛋白质翻译与加工,神经氨酸酶抑制剂阻止病毒组装与释放。针对不同病毒周期开发药物,有望降低耐药性。
随着结构生物学(如冷冻电镜技术)的发展,解析病毒关键蛋白及其与宿主蛋白相互作用的高分辨率结构成为可能。这为基于结构的药物设计(SBDD)提供了坚实基础。例如,通过解析SARS-CoV-2 Mpro的三维结构,科学家们能精准设计与其活性口袋紧密结合的抑制剂。同时,机器学习和人工智能技术被用于分析病毒基因组和蛋白质序列特征,辅助预测潜在的药物靶点,提高筛选效率。
整合基因组学、转录组学、蛋白质组学和代谢组学等多组学数据,有助于构建病毒感染的复杂网络模型,识别病毒与宿主互作网络中的核心节点和瓶颈环节,这些往往是理想的药物干预靶点。例如,研究病毒感染引起的宿主细胞代谢重编程,可能发现调控关键代谢酶的新靶点。
面临的挑战与策略
尽管已有多种抗病毒药物用于治疗,但是其研发仍面临残酷的挑战。
01病毒结构和周期
病毒的结构和生命周期相对复杂,部分病毒的复制机制尚不明确,影响了基于靶点的抗病毒药物研发。病毒复制和感染宿主细胞的过程为药物开发提供机会,但病毒仅编码自身的几种蛋白质,靶点可能只有一个或少量数个。有些蛋白还可能具有宿主细胞的功能,靶向这些蛋白可能会伤害健康人体细胞,这是抗病毒药物开发的难点之一。
研究人员在安全靶向病毒关键蛋白方面进行大量研究,如HIV中的整合酶、RNase H、核衣壳蛋白7,乙型肝炎病毒的核糖核酸酶,流感病毒核酸内切酶。这些负责DNA或RNA复制的聚合酶在多种病毒中具有相似的位点,因此是开发广谱抗病毒药物的研究方向。
02病毒变异与耐药性
病毒,尤其是RNA病毒,具有高突变率,导致靶点药物失效。这一点在抗SARS-CoV-2药物开发中彰显的淋漓尽致。SARS-CoV-2的持续突变一直是人们关注的重点,特别是Omicron突变体的出现,相较于原始毒株,其基因组发生了30多个突变。这些突变增强病毒的传播性和抗药性。病毒非结构蛋白的突变会提升其适应能力,增加感染率,如RdRp上的S759A和V792I等突变导致病毒对瑞德西韦的耐药性。
开发抗耐药性抑制剂是积极应对病毒突变的策略之一。Mpro是病毒生命周期中不可或缺的蛋白水解酶,在冠状病毒中高度保守,且人体内缺乏同源蛋白酶,因此成为抗SARS-CoV-2药物设计的理想靶点。
03缺乏合适的动物模型
缺乏能够有效表征临床症状的动物模型,也增加了药物研发的难度。抗病毒药物发现并不仅限于设计好的抑制剂,还要证明药物有限,首先是在细胞中,然后是动物模型,最后才是人类。但细胞和动物模型的差异会给病毒研究带来障碍。
不同病毒、甚至同种病毒的不同毒株对药物的敏感性差异巨大。建立更精准的体外模型和动物模型,以及开展严谨的大规模临床试验至关重要。类器官技术的发展则提供了更贴近临床实际模型。
义翘神州抗病毒药物开发靶点蛋白
随着构生物学、生物信息学、蛋白质组学和反向遗传学等技术的进步,研究人员对病原体的结构和生命周期有了更深入的理解,显著提高药物研发的速度和成功率。此外,靶向蛋白降解、共价药物、核酸药物等技术的发展,对开发多维度、多靶点药物提供新的解决方案。
义翘神州已自主开发了一系列高质量的抗病毒药物靶点,包括新冠小分子药物靶点RdRp、3CLpro、NSP7、NSP8、NSP10、NSP13 (Helicase)、NSP14 (Exonuclease)、NSP16 (Methyltransferase) 等,以及猴痘、流感、RSV和HIV等的关键靶点,全面支持抗病毒药物开发。






