北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
实验室数据完整性风险评估:我们如何守住检测结果的“生命线”?
86 人阅读发布时间:2026-03-31 09:21
在第三方检测实验室,数据完整性(Data Integrity,DI)不仅关乎信任与合规,更是实验室生存发展的“生命线”。无论是电子记录还是纸质记录,数据的真实性、完整性和可追溯性,直接决定了检测结果的可靠性、客户的信任度,甚至官方检查的成败。
随着业务规模的持续扩张,实验室普遍采用电子与纸质并存的“混合记录模式”,使数据生成、处理、存储的复杂性显著提升。与此同时,国内外监管机构(如FDA、EMA、NMPA)对数据完整性的要求日趋严格,ALCOA+原则已成为衡量实验室合规水平的“金标准”。在这样的监管环境下,如何建立一套经得起推敲的数据管理体系,成为每一位质量管理人员都要面对的严峻课题。
为满足客户对检测数据真实性的高期待、提前识别并消除审计中的常见缺陷,并建议一套经得起推敲的数据管理体系,我们近期开展了一次覆盖全流程的质量风险评估。本次评估采用失效模式与影响分析(FMEA)方法,系统梳理了数据生命周期中的潜在风险点,并制定了针对性的控制措施。
本次评估覆盖实验室所有检测业务范围内的记录和数据类型,包括电子数据和纸质数据两大类别,采用失效模式与影响分析(FMEA)方法,从三个维度对风险进行量化评分:
· 严重性(S):风险对数据完整性的影响程度
· 发生概率(O):风险发生的可能性
· 可检测性(D):风险是否容易被发现
各维度按照1-5分进行赋值,根据风险优先数(RPN)(RPN=S×O×D)客观评估各类风险的优先级,以及采取相应的措施,为后续的资源配置和改进决策提供科学依据。
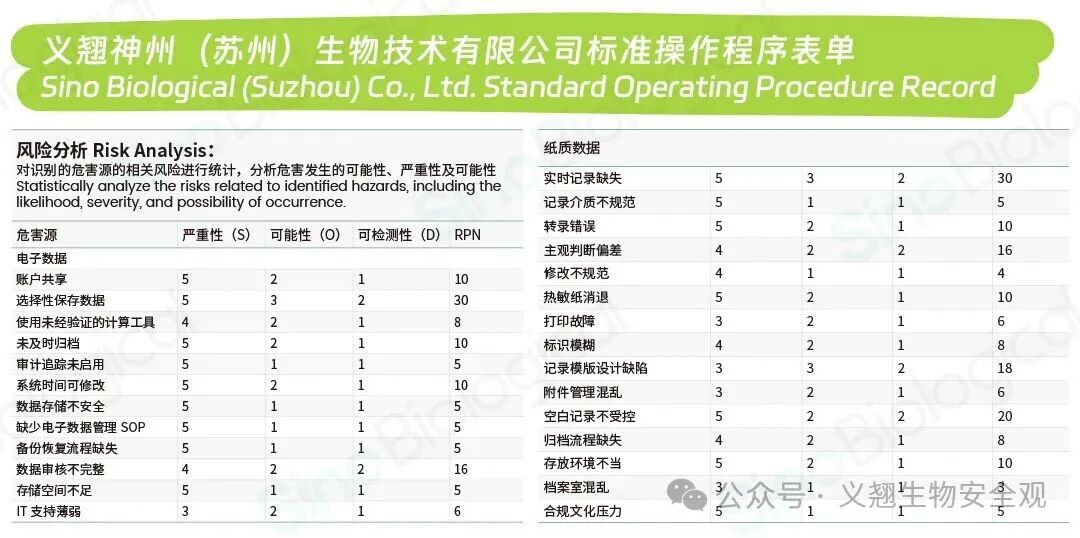
在电子数据管理方面,我们识别出多项值得关注的风险点,其中最为突出的包括:
· 账户共享:多名人员共用同一账户,导致操作无法追溯至具体责任人
· 选择性保存数据:仅保留“合格”结果,删除异常数据,导致数据不完整
· 未经验证的计算工具:如Excel表格公式可随意修改,计算错误无法追溯
· 审计追踪未启用:关键数据变更缺乏可追溯的电子记录
· 系统时间可修改:破坏数据时序逻辑,无法证明操作的真实发生时间
· 备份机制缺失:灾难发生时无法有效恢复数据
· 数据审核不完整:仅审核纸质报告,未同步审核电子原始数据和审计追踪
纸质记录作为传统的数据载体,同样面临诸多管理挑战:
· 实时记录缺失:事后补记导致关键信息遗漏或失真,无法还原操作过程
· 记录介质不规范:如使用铅笔,数据易被篡改,失去原始性
· 转录错误:抄录过程出现差错,原始草稿通常不保存,造成追溯链断裂
· 修改不规范:涂改处未签注日期及原因,易引发造假质疑
· 热敏纸消退:字迹随时间自然消失,无法满足数据持久性要求
· 标识模糊:外包装、标签脱落或模糊,导致物料信息无法辨认
· 记录模板设计缺陷:字段设置不合理,易引发漏填或错填
· 空白记录不受控:版本管理混乱,一致性和规范性无法保证
通过对所有识别出的风险点进行风险优先数(RPN)评分,我们得出了明确的风险分级结果:
电子数据风险整体处于低水平(1≤RPN≤24),但部分仍需重点关注,如选择性保存数据。
纸质数据风险中,“实时记录缺失”被评定为中风险(25≤RPN≤74),需优先改进。此外,“记录模板设计缺陷”、“空白记录不受控”等问题亦需持续优化。
针对本次评估中识别的数据风险,我们将从人员、流程、技术、审核等多个方面进行提升:
· 加强人员培训:系统提升全员对数据完整性要求的认知水平与操作规范性
· 优化管理流程:完善电子数据管理标准操作规程(SOP),规范纸质记录全流程管理
· 推进技术升级:启用审计追踪功能、锁定系统时间权限、建立自动化备份与恢复机制,并上线文档管理系统(DMS)及培训管理系统(TMS)电子化系统
· 强化审核机制:建立电子原始数据与纸质报告的同步审核机制,确保数据全程可追溯
· 改善存储环境:确保纸质记录和电子数据的存放环境安全、持久、合规
数据完整性建设难以一蹴而就,它需要制度、技术、文化的协同支撑。通过本次质量风险评估,我们不仅系统梳理了潜在风险,更明确了未来改进的方向和路径。
未来,义翘神州将持续推进数据管理的标准化、系统化和智能化,确保每一份检测报告都能经得起时间与监管的考验,为客户提供值得信赖的检测结果,为生物安全事业贡献专业力量。






