北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.20000000000000018
- 0.20000000000000018
- 2.2
- 2.2
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
一文读懂ELISpot:原理、实验应用全解析
35 人阅读发布时间:2026-03-26 15:41
什么是ELISpot?
ELISpot的全称是Enzyme-linked Immunospot Assay(酶联免疫斑点技术)。这个名字本身就暗藏玄机,既不是ELISA的简单升级,也非普通细胞培养实验,而是将两者巧妙融合后诞生的单细胞功能检测技术。
ELISpot的原理是:免疫细胞被刺激物激活,分泌细胞因子或免疫球蛋白,而ELISpot板底的PVDF膜上包被有特异性抗体,能够捕获免疫细胞的分泌物。然后通过免疫酶联标记技术将包被抗体捕获的细胞因子以斑点的形式显示出来。简单来说就是“酶联免疫”加“斑点”。
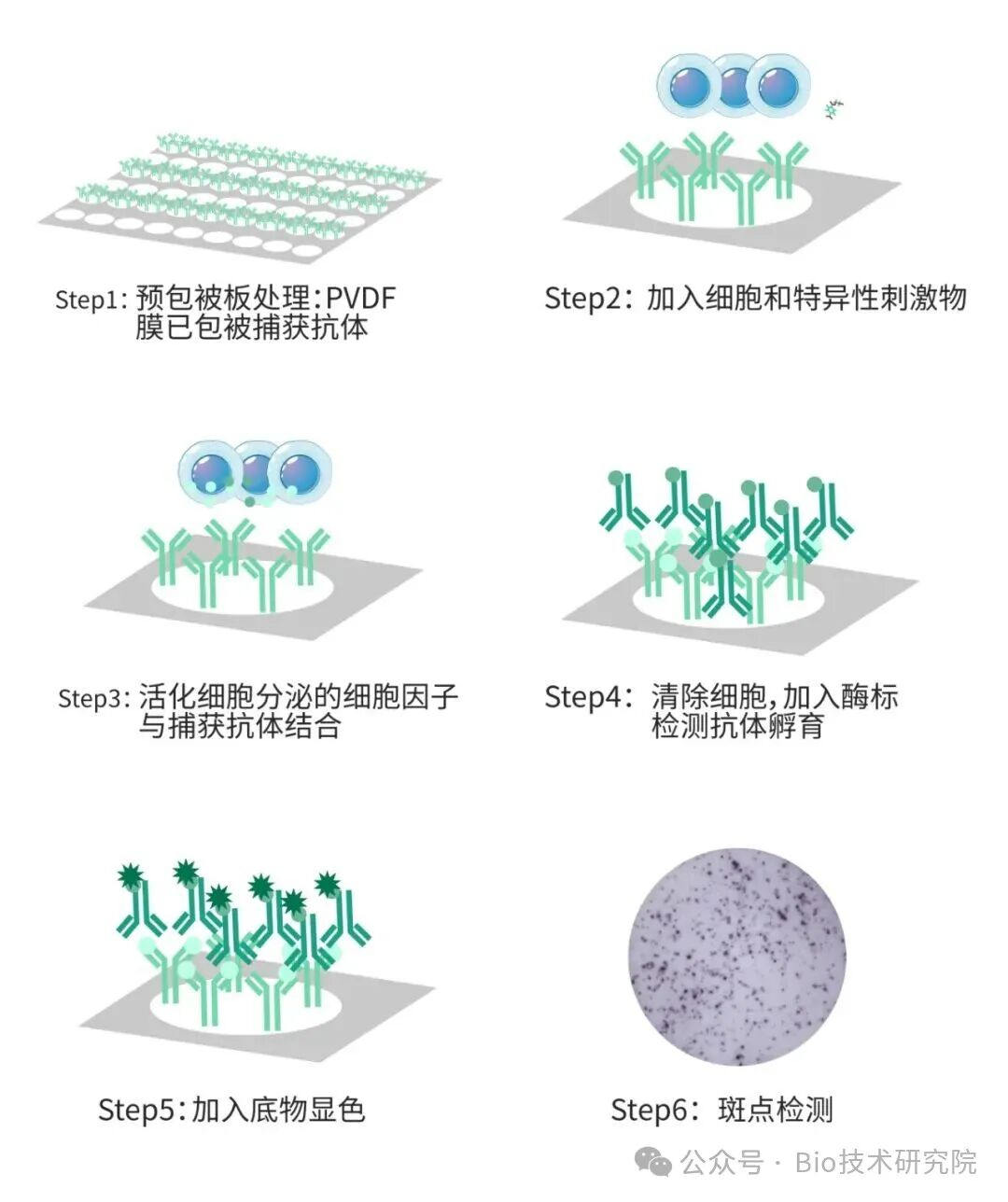
ELISpot技术核心原理可以概括为四步:
1,ELISpot实验可以在96孔上进行,每个板孔底部(常为平底)铺有一层PVDF膜。膜上包被高特异性的单克隆抗体,用于捕获细胞分泌的细胞因子。
2,将待测细胞和刺激物进行共培养。待测细胞为PBMC、脾细胞、肿瘤浸润淋巴细胞等活细胞。刺激物可以是伴刀豆蛋白A(ConA)、多肽、重组蛋白、CD3抗体等。在刺激物作用下,免疫细胞会在对应的时间段分泌对应的细胞因子。细胞因子将会被包被在膜上的抗体特异性捕获。
3,清除细胞,加入生物素标记的二抗,进行酶联反应。
4,加入底物显色,在膜上形成肉眼可见的斑点。一个斑点代表一个阳性细胞,通过读板仪器可以统计阳性细胞数量。阳性细胞率(%)=(膜上斑点数/孔内细胞总数)×100%
哪些实验可用到ELISpot?
ELISpot基于细胞培养和ELISA技术,能够在单细胞水平上检测细胞因子的分泌表达功能。其原理是利用抗体捕获培养中的细胞分泌的细胞因子,通过酶促反应将其结果显示出来。ELISpot技术灵敏度高,比传统的ELISA高2-3个数量级(即100-1000倍)。
目前已有商业化检测细胞因子的ELISpot检测试剂盒。可检测细胞因子有干扰素(IFN-γ)、白介素(IL-2、IL-4、IL-5、IL-6、IL-10等)、颗粒酶(Granzyme B)、肿瘤坏死因子(TNF-α)等,可检测的样品种属有人、小鼠、大鼠、猴子等。随着技术的发展,双色、多色及荧光ELISpot方法也将会得到进一步开发。
ELISpot设计之初是用于检测B淋巴细胞分泌抗体的水平。B细胞分泌抗体一般量较大,容易检测,即时早期ELISpot灵敏度不高也能满足需求。随着技术进步,ELISpot检测灵敏度越来越高,因此更多地用于细胞因子检测。
目前,ELISpot广泛用于免疫研究领域,如T/B细胞功能研究、自身免疫检测、疫苗研究、肿瘤免疫治疗开发、基因疗法免疫原性检测等。
怎么进行ELISpot?
接下来我们以义翘神州的小鼠IFN-γ ELISpot试剂盒(ALP)(货号:EK50709A)为例,分享ELISpot实验操作步骤。
整个过程可以概括为以下三步:
1,预包被板处理(无菌操作)
2,细胞培养(无菌操作)
3,斑点检测(不需无菌操作)
第1天-预包被板处理,接种细胞共培养(严格注意无菌操作)
需自备试剂或仪器:
RPMI-1640培养基(或无血清培养基)、胎牛血清(FBS)、无菌PBS洗液,超净工作台、低温离心机、CO2培养箱、微量移液器及配套Tip枪头、8通道微量移液器、0.5mL和1.5mL EP管、过滤器、细胞计数器、酶联斑点分析仪等。
配制试剂:
1)阳性刺激物:按照刺激物使用说明书和本次实验用量,现用现配。
2)配制适量含5%-10%胎牛血清(FBS)的RPMI-1640培养基。
操作步骤:
1. 预包被板处理(无菌操作)
1)从密封包装中取出预包板,用无菌PBS洗涤4次(200μl/孔)。
2)用含有5%-10%胎牛血清(FBS)的无菌RPMI-1640培养基(200μl/孔)对预包板进行处理,室温孵育至少30分钟。
2. 细胞培养(无菌操作)
1)弃掉孔内液体,拍干,每孔先加入100μL的刺激物。背景对照孔和阴性对照孔不加刺激物,分别加入200μL和100μL的无菌RPMI-1640培养基。
2)在阳性、阴性对照孔及实验孔中加入稀释好的细胞悬液(100μL/孔)。
注意:细胞悬液和刺激物的浓度应根据实际情况进行调整,各组设置建议如下:
✦ 背景对照组:不加细胞悬液和刺激物,仅加培养基。
✦ 阴性对照组:不加刺激物,加入和实验组细胞数量一样的细胞悬液。
✦ 阳性对照组:加入工作浓度的阳性刺激物,如刀豆蛋白A(ConA)常用浓度为0.25-2.5μg/mL。建议加入的细胞数比实验组少,如1 x 105 cells/孔。
✦ 实验组:根据实验设计加入合适浓度的刺激物。刺激物可用无血清培养基或者RPMI1640 配制成10倍储存液,使用时用培养基稀释至1倍浓度。建议细胞总数为1.5-2.5 x 105 cells/孔。
建议在进行ELISpot实验时设置2-3个复孔。
3)细胞培养孵育:
加样完成后,盖好板盖,放入37℃、5% CO2培养箱静置培养18-48h。孵育期间避免晃动或移动板子,建议用封口膜或铝箔纸封严,避免蒸发。
Tips:
① 加入细胞后,不要震动或拍击ELISpot板,防止细胞成圈分布在孔的外周,不利于斑点形成。培养时ELISpot板间不能叠放,叠放可能会造成整块板温度不均匀,出现边缘效应。板的碰撞或移动还可能会造成细胞移位,导致斑点模糊、拖尾、一个细胞生成多个斑点等。
② 细胞状态直接影响ELISpot检测结果,需选用细胞状态好、活力高、功能保持完成的细胞进行实验。新鲜分离的原代细胞,需尽量减少分离过程中的机械损伤及有害化学物质对细胞的损害。冻存复苏的细胞,可在37°C新鲜培养基中放置1小时或更长时间,提高细胞性能。
第2天-斑点检测
配制试剂:
Tips:以下试剂均需现用现配。PBS应用0.2µm滤膜进行过滤。在洗涤和孵育缓冲液中避免使用吐温或其他去污剂。
检测抗体:按说明书推荐倍数,用含有0.5% FBS的PBS(PBS-0.5% FBS)稀释检测抗体。如义翘神州小鼠IFN-γ ELISpot试剂盒(ALP)(货号:EK50709A)建议按照1:350稀释检测抗体。建议用0.2µm滤膜过滤。
链酶亲和素(Streptavidin-ALP):按说明书推荐倍数,用含有0.5% FBS的PBS(PBS-0.5% FBS)稀释Streptavidin-ALP,如用PBS-0.5% FBS按照1:170稀释。建议用0.2µm滤膜过滤。
显色液:显色液配制比较繁琐,一定要看清试剂标签。如小鼠IFN-γ ELISpot试剂盒(ALP)中,需将BCIP/NBT-plus溶液A与稀释液按1:250的体积比进行混合,然后加入与溶液A等体积的溶液B,即BCIP/NBT-plus溶液A、稀释液、溶液B的体积比为1:250:1。建议用0.45µm滤膜过滤。
操作步骤:
1. 低渗裂解细胞:从培养箱中取出ELISpot板,弃掉孔内液体,在滤纸上拍干。然后在每孔中加入200μL 4°C预冷的去离子水,置于4°C冰箱10min。
Tips:利用去离子的水低渗作用诱导细胞膨胀和裂解,更容易在洗板过程中将其去除,否则会影响斑点的形成。
2. 洗板:完成裂解后,弃掉孔内液体并拍干。接着每孔中加入200μL无菌的PBS,浸泡1min。然后弃掉孔内液体,拍干。重复洗板操作5次。
3. 检测抗体孵育:每孔加入100μL稀释好的检测抗体,室温条件下孵育2h。
4. 洗板:抗体孵育结束后,弃掉孔内液体并拍干。然后向每孔中加入200μL无菌的PBS进行洗板。重复洗板5次。
5. Streptavidin-ALP孵育:每孔加入100μL稀释好的Streptavidin-ALP,室温条件下孵育1h。
6. 洗板:抗体孵育结束后,弃掉孔内液体并拍干。然后向每孔中加入200μL无菌的PBS进行洗板。重复洗板5次。
7. 显色:每孔加入100μL底物显色液,室温避光孵育5-30 min,根据斑点生成情况选择终止显色时间。
Tips:显色反应通常发生在10-30 min,通过目视监测斑点的形成过程。
8. 终止反应:待斑点出现后,用大量自来水或去离子水冲洗。建议揭开板底座,冲洗膜的底部。
9. 读数:将ELISpot板放置在室温阴凉处,待板完全干燥后再进行读数。可使用斑点分析仪或显微镜进行斑点计数及分析。
Tips:请勿在高于37°C的温度下干燥膜板,否则可能导致膜破裂。斑点计数时,应注意区分由纤维、膜撕裂、碎片等导致的不规则斑点,一般细胞生成的斑点通常为圆形。






