北京义翘神州科技股份有限公司(Sino Biological Inc.)品牌商
17 年
手机商铺
- NaN
- 0.2999999999999998
- 0.2999999999999998
- 2.3
- 2.3
北京义翘神州科技股份有限公司(Sino Biological Inc.)
入驻年限:17 年
- 联系人:
客服部
- 所在地区:
北京
- 业务范围:
技术服务、试剂、抗体、细胞库 / 细胞培养、ELISA 试剂盒
- 经营模式:
生产厂商
推荐产品
公司新闻/正文
肿瘤类器官如何“替身试药”,迈入癌症精准治疗新纪元【附培养与鉴定指南】
348 人阅读发布时间:2025-05-27 15:06
01 引言:类器官前进的步伐加快
类器官已经成为科研界的热门领域,据PubMed搜索数据显示,2024年“Organoid”相关的文章数量是2020年2倍多,更是十五年前的10倍。尤其在今年4月份,美国FDA发布颠覆性公告,将逐步取消动物实验的强制要求,支持类器官验证结果,这必将进一步加快类器官行业的发展步伐。
类器官是具有一定空间结构的组织类似物,能够在结构和功能上模拟真实器官。因此,类器官在器官发育、精准医疗、再生医学、药物筛选、基因编辑、疾病建模等领域都有广泛的应用前景。
义翘神州紧随类器官的发展步伐,自主开发类器官培养、分化、分析和鉴定所需的细胞因子、生长因子、小分子化合物及抗体等产品。我们现推出正常组织和肿瘤类器官培养与鉴定指南,欢迎下载查看。
点击查看或下载 → 正常组织类器官培养与鉴定指南
点击查看或下载 → 肿瘤类器官培养与鉴定指南
02 迭代:从生理组织到肿瘤类器官
肿瘤类器官已成为患者来源组织的理想体外模型。传统的2D培养仅限于形成细胞单层,在传代过程中会失去原有的生理功能。源自不同物种和品系的动物模型具有不同的生理特征和反应,存在高异质性。
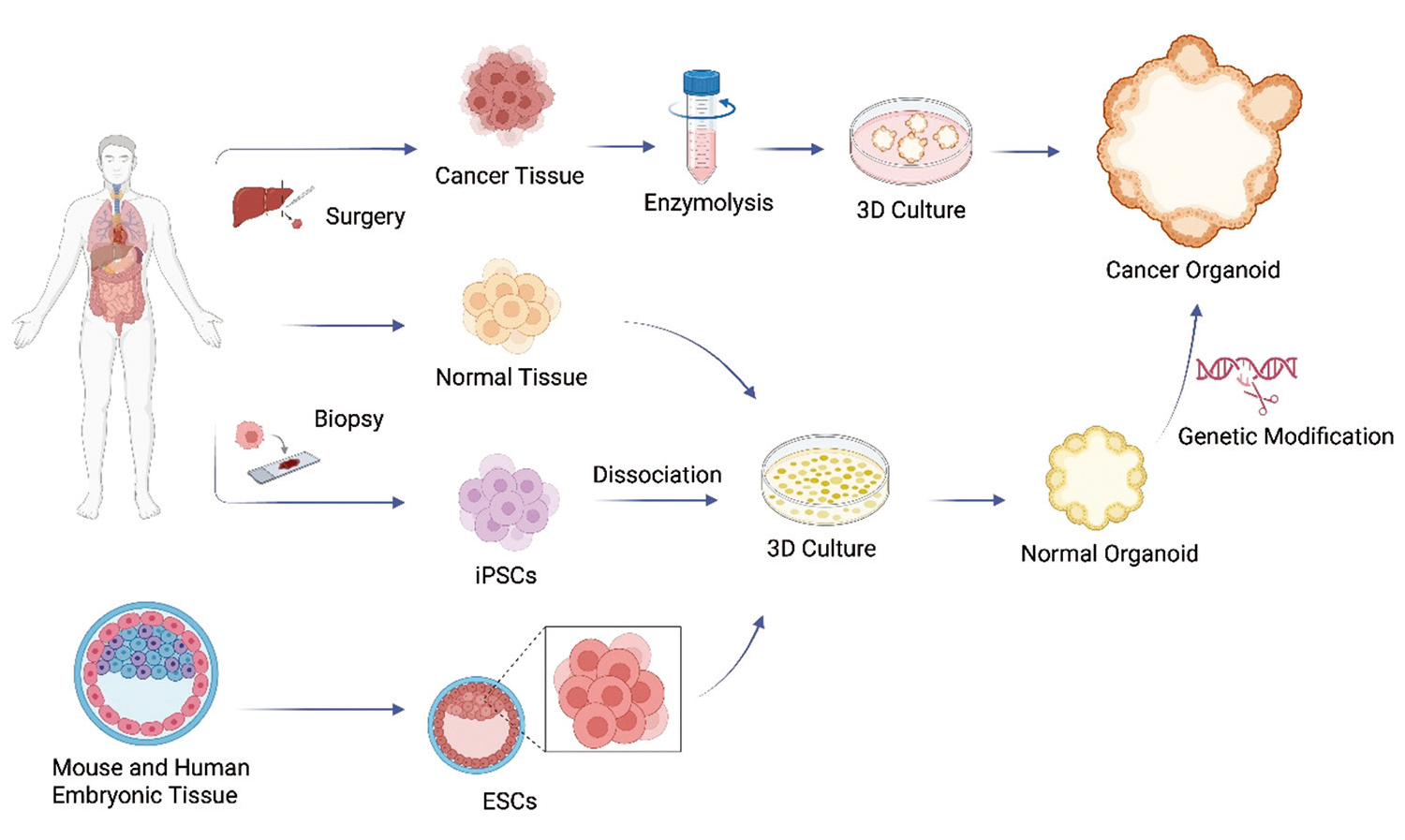
肿瘤类器官构建基本方案
(源自文献:doi: 10.36922/OR025050008)
类器官不仅支持干细胞的自我维持和分化,可以更好的模拟人体生理环境,维持细胞的增殖、凋亡和分化等生理功能。肿瘤类器官还可以添加对应癌症类型的特异性细胞因子,构建具有体外微环境的肿瘤模型,除了直接再现肿瘤生长过程,还可再现肿瘤组织的特征,更精准捕捉个体间差异,为个性化肿瘤治疗提供基础研究。
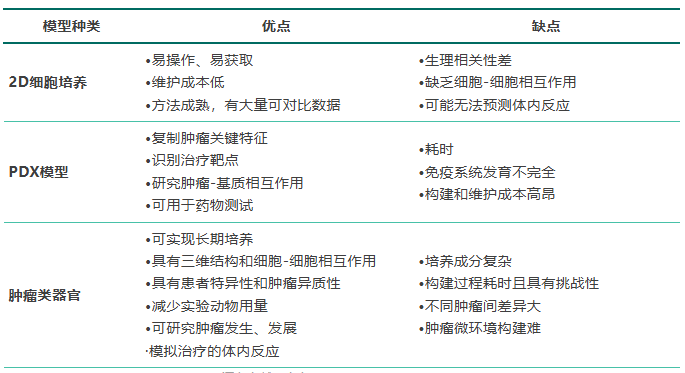
源自文献:doi: 10.36922/OR025050008
03 突破:肿瘤类器官培养技术
肿瘤类器官培养体系包括基质凝胶和维持类器官生长的细胞因子混合物。
基质凝胶主要有胶原蛋白、巢蛋白、层粘连蛋白和其他成分组成,用作肿瘤细胞的3D支架。这种仿生环境模拟体外细胞与胞外基质相互作用,提供细胞聚集、增殖和迁移的条件,从而准确模拟人体的内部环境。
肿瘤类器官模型的成功构建还依赖于补充细胞因子和小分子化合物。有两条信号通路直接影响类器官的生长:EGFR和Wnt。激活EGFR通路能够促进癌细胞增殖,这需要在培养基补充EGF。Wnt通路的刺激需要R-Spondin和Wnt-3a,参与控制细胞增殖、黏附、分化等过程。
比如在肺癌培养体系中,需要添加EGF、R-Spondin、Wnt-3a、Noggin等,以促进类器官增殖和维持干性。而在结直肠癌类器官培养中,由于存在Wnt通路的激活突变,培养基中不需要再添加R-Spondin和Wnt-3a。FGF7、FGF10是促进干细胞向细胞谱系远端分化所必需的。
除此之外,一些激酶抑制剂的小分子化合物也会用于类器官培养,如间变淋巴瘤激酶(ALK)抑制剂A83-01、Rho激酶(ROCK)抑制剂Y-27632、糖原合成酶激酶-3(GSK-3)抑制剂CHIR-99021、丝裂原活化蛋白激酶(MAPK)抑制剂SB-202190等。
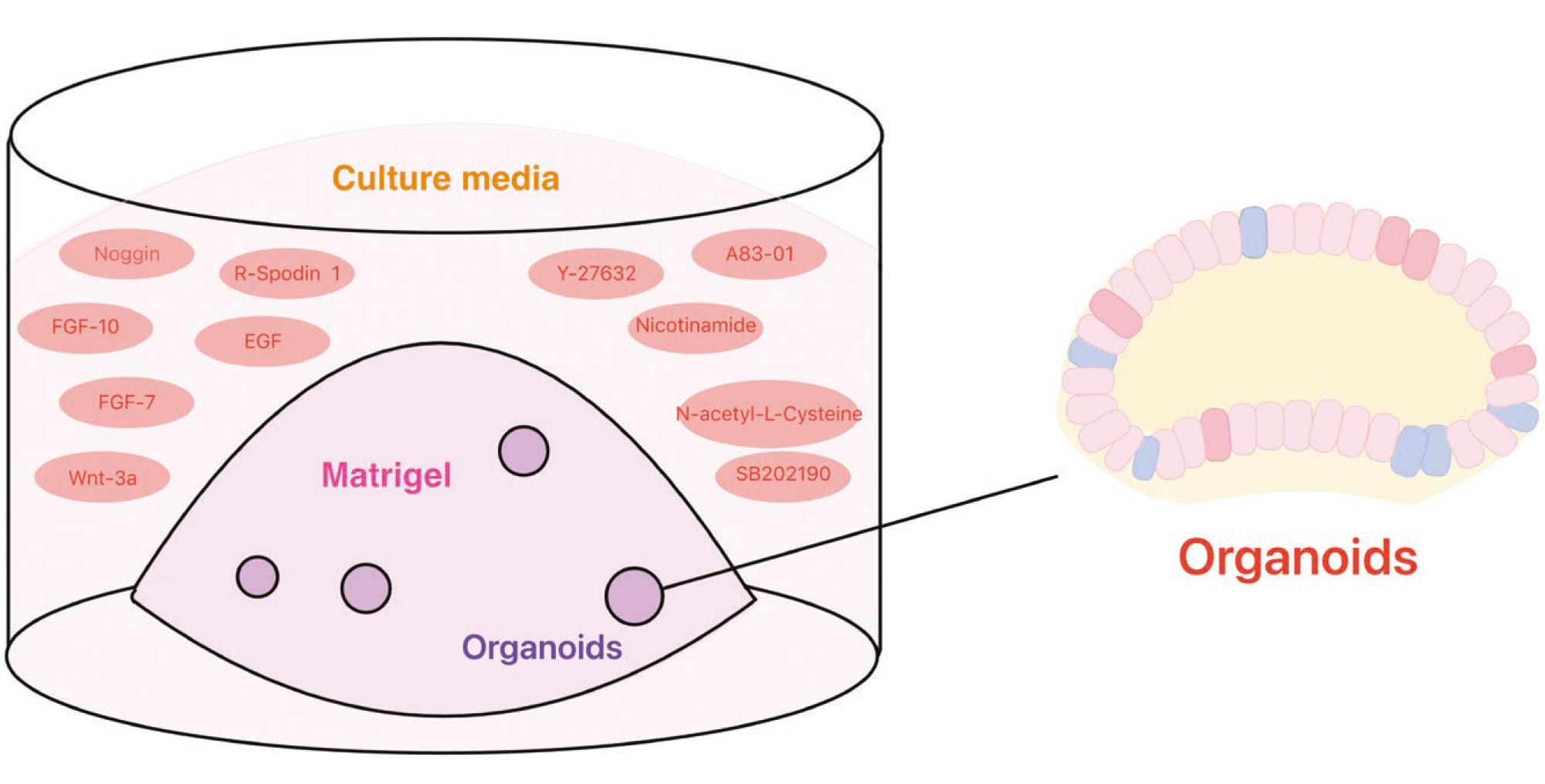
类器官培养体系
(源自文献:doi: 10.1093/stmcls/sxae070)
肿瘤类器官培养体系中添加哪种细胞因子以及何时添加,都需要开展额外实验,构建每种癌症组织学亚型的最佳培养体系。由于肿瘤组织来源不同,添加细胞因子和小分子化合物比使用血清费时费力,需要根据每个组织的特性进行调整。
香港大学的Suet Yi Leung团队在“Organoid cultures for cancer modeling”综述中,对不同器官来源(正常或癌症)的类器官模型构建所需的细胞因子和小分子化合物进行了汇总。Wnt3a、R-spondin 1、EGF、FGF等细胞因子用于不同来源的类器官培养中。
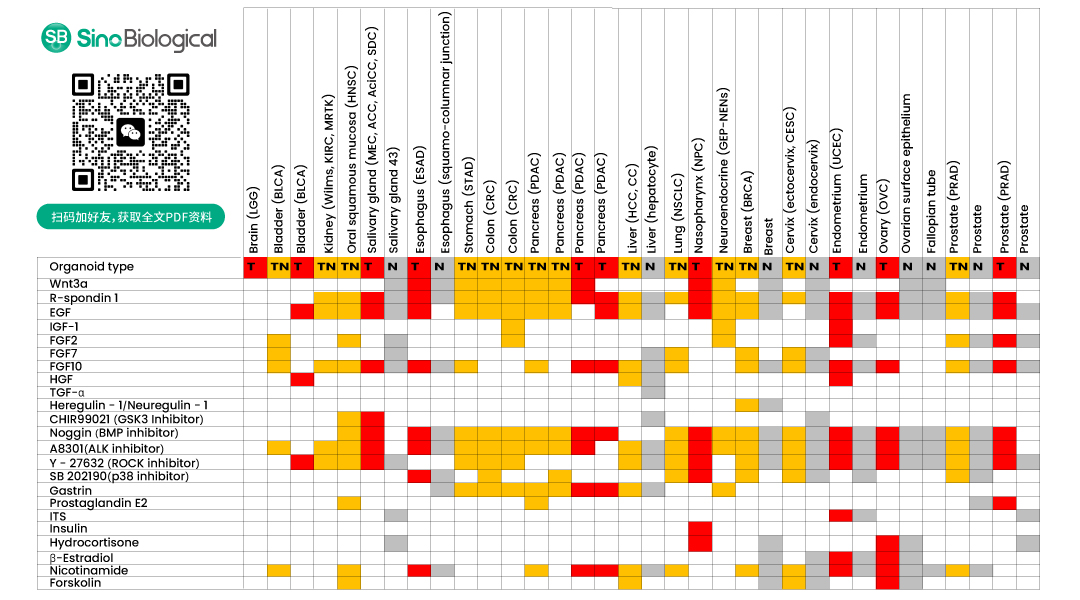
正常器官或癌症来源的类器官培养中常用的细胞因子和小分子汇总表(源于文献:doi: 10.1016/j.stem.2023.05.012)
义翘神州类器官解决方案
类器官构建需要一系列操作步骤,如采样、培养、后续评估鉴定。义翘神州作为一家专注于为全球生物医药领域提供生物试剂和技术服务的高新技术企业,成功开发类器官培养、分化、分析和鉴定所需的细胞因子、生长因子、小分子化合物及抗体等产品。现推出全面的类器官解决方案,涵盖多种生理和病理类器官模型,全力支持您的类器官培养与鉴定。
【参考文献】
1. Cao L, et al. Application of cancer organoids: The forefront of personalized oncology and preclinical testing. Organoid Res. 2025, doi: 10.36922/OR025050008
2. Jianing Zuo,et al. High-throughput solutions in tumor organoids: from culture to drug screening. Stem Cells. 2025
3. Helen H.N. Yan, et al. Organoid cultures for cancer modeling. Cell Stem Cell. 2023
4. Lucie Thorel, et al. Patient-derived tumor organoids: a new avenue for preclinical research and precision medicine in oncology. Experimental & Molecular Medicine. 2024







